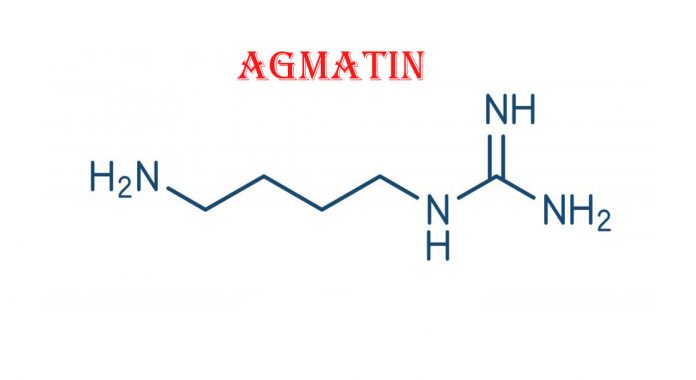
Agmatin Nedir Ve Ne İşe Yarar ?
Agmatin, L-Arginin’in bir metabolitidir. Nöropatik ağrı ve uyuşturucu bağımlılığını hafifletmek için vaat ettiğini gösterir. Agmatin supplementi ayrıca bilişsel sağlığada faydası olabilir.
Özet
Tüm Temel Faydalar / Etkiler / Gerçekler ve Bilgi
Ön araştırmalar, agmatinin nöropatik ağrı ve uyuşturucu bağımlılığı tedavisinde potansiyel bir kullanımı olduğunu öne sürüyor. Aynı zamanda beyni toksinlerden ve felç’den korur.
Agmatinin kendiliğinden desteklenmesi ağrı algısını artırabilir, ancak morfin ve fentanil gibi ağrı kesiciler ile sinerjik çalışır. Agmatin’in opioidler ile olan sinerjisi ağrı kesici toleransını, bağımlılık olasılığını ve ağrıyı azaltmasına olanak tanır.
Agmatin’in çeşitli mekanizmaları vardır. N-metil-D-aspartat (NMDA) ve nikotinik asetilkolin reseptörlerini bastırabilir, aynı zamanda imidazolin reseptörlerini de aktive edebilir. Agmatin, nitrik oksit sentez enzimlerini de bastırabilir ve böylece yüksek nitrik oksit seviyelerini düzenler. Agmatin, kalsiyum kanallarını ve bazı serotonin reseptörlerini de engelleyebilir. Agmatinin mekanizmalarının tam boyutunu belirlemek için daha fazla araştırmaya ihtiyaç vardır.
Agmatin’in oldukça umut verici bir araştırma kimyasalı olduğunu önermek için bir sürü hayvan kanıtı var. Genel bir supplement değildir, çünkü etkileri için insan kanıtlarının eksikliği vardır. İnsanlar üzerinde çeşitli çalışmalar yapılmıştır, ancak çoğunluk agmatin enjeksiyonlarını kullanır, oral yoldan alınmamaktadır. Araştırmalar, agmatin’in geniş yelpazedeki takviyenin göz önüne alınması için oral yoldan alınmasının etkilerini göreceğini ortaya koymalıdır.
Bilmen Gerekenler
Agmatin Ayrıca şöyle bilinir
Klonidin değiştiren madde, 4- (aminobütil) guanidin, dekarboksilatlı arginin
Şaşırmayın
L-Arginin (eş yapısı)
Dikkat Edilmesi Gerekenler
Agmatin zamanında şu anda oldukça toksik görünmese de, süper yüklemenin yetersiz toksikolojik testleri yapılmasına rağmen, insanlarda kullanılan 2.670 mg dozaja uymak akıllıca olabilir.
Agmatin Aşağıdakilerin Bir Formudur
- Amino Asit Desteği
- Nootropik
Agmatin Aşagıdakiler İle Gider
- Bupropion (farmasötik antidepresan; agmatin etkinliğini arttırır)
- Opioidergik ağrı kesiciler (morfin gibi)
- Agmatin olarak kanabinoidler (marihuana gibi), kanabinoid (CB1) reseptörü
- Alkol yoksunluğu (semptomları azalttığı görülüyor)
Agmatin Aşagıdakiler İle İyi gitmez
- L-Arginin ve L-Sitrülin (bazı nörolojik etkiler için, iyi aydınlatılmamış kardiyovasküler etkileşimler için)
- Yohimbine ve Rauwolscine (Agmatin, bastırdığı α2A reseptörünü aktive eder)
- D-Aspartik asit NMDA reseptörleri vasıtasıyla sinyal azaltılmasına bağlıdır
- Alkol birleşimi (alkolden ülser oluşumunu artırabilir)
- Kreatin (kreatinin pozitif olarak NMDA sinyalini etkilediği varsayılarak, agmatin aynı yerde ters yönde çalışır; kas büyümesi veya nitrik oksit artışı için zıt olmamalıdır)
Agmatin Tarihi
Agmatin, 1910 yılında Albrecht Kossel tarafından keşfedilmiştir. Kimyasalın tam işlevlerini bulmak 100 yıldan fazla sürdü. Bu terim, a- (amino için) + g- (guanidin’den) + -ma- (ptomaine’den) + -in (Almanca) / – ine (İngilizce) ekinin -t-görünüşte euphony için eklenmesiyle ortaya çıkar. Keşfedilmesinden bir yıl sonra, Agmatinin tavşanlarda kan akışını arttırabildiği bulunmuştur, ancak gerekli olan yüksek konsantrasyonlar (yüksek μM aralığı) göz önüne alındığında, bu bulguların fizyolojik önemi sorgulanmıştır. 1920’lerde, Oskar Minkowski’nin diyabet kliniğinde bulunan araştırmacılar, agmatinin hafif kan şekeri düşürücü etkiler gösterebileceğini göstermiştir. 1994 yılında, memelilerde dahili agmatin sentezi keşfi gerçekleşmiştir.
Agmatin Nasıl Kullanılır Ve Kullanımı Nedir ?
Agmatin etkileri için insan kanıtlarının eksikliği nedeniyle standart dozajlar yoktur. Bununla birlikte, tek bir insan çalışması nöropatik ağrı tedavisinde günlük 1,300-2,670 mg agmatin kullanımı vardı. Bilişin iyileştirilmesi için tahmini insan dozu oral yolla 1.6-6.4 mg / kg Agmatin olarak kullanılır. Bu, sıçanlar için 10-40 mg / kg dozaj aralığına dayanır ve 60 kilo kişi için 217-435 mg’a eşdeğerdir. Suplementasyon, vücut ağırlığının kilogramı başına 6.4 mg’ı geçmemelidir.
Agmatin yönelik çalışmalar günlük dozlama protokolünü kullanır. Agmatin, diyet proteini ile alındığında iyi emilmez, çünkü arginin aynı taşıyıcıları kullanır. Oral agmatin takviyesinin hayvan çalışmalarında gözlemlenenlerle aynı faydaları sağladığını belirlemek için daha ileri araştırmalara ihtiyaç vardır.
| KANIT SEVİYESİ | Sonuç | Notlar | ||
|---|---|---|---|---|
| Ağrı | Bel diskine bağlı radikülopati üzerine yapılan çalışmada, ağrı hafifletme derecesi, plaseboya göre oldukça dikkat çekiciydi ve supplement tamamlandıktan iki ay sonra da devam etti. Maalesef referans ilaç karşılaştırmaları yok | |||
| Depresyon | Bir çok ön çalışma mevcut, ancak 2-3 g agmatin içeren üç konuda da hafifletme sağlandı. |
1 Kaynaklar ve Yapı
1.1. Kaynaklar (Nerelerde ve Hangi Besinlerde Bulunur)
Agmatin, L-Arginin’in bir dekarboksile edilmiş formu olan ve 4- (aminobütil) guanidin moleküler ismini taşıyan bir moleküldür (özellikle biyojenik amin, [1]); [2] Agmatin olarak isimlendirilmesinden önce, Bağlı Clonidin’in (yüksek tansiyon tedavisinde kullanılan bir ilaçtır) reseptörlerden yer değiştirdiği keşfedilen “Clonidin yer değiştiren madde” olarak tanımladı. [3]
Agmatin, insan vücudunda bir sinyal molekülü olarak işlev görebilen küçük bir biyojenik amindir; L-argininin amino asidinin dekarboksilatlanmış halidir.
Agmatin bakteryal olarak ifade edilen argininden agmatin üreten enzim dönüşümünde ötürü bir bakteriyel yan ürünüdür ve bu gibi fermente edilmiş gıdalarda bulunur: [4]
- Beyaz şarapta 6.5ppm, kırmızı kırmızıda 22ppm kadar şarap [5] [6]
- 0.5-42ppm’de bira [7] [8] [9]
- Sake (bir japon içkisi) 114ppm [10]
- 0,4-5,3ppm’de kahve (anlık) [11]
- Karasal et ürünleri (normalde 3.1ppm, pişirildikten sonra 27ppm’ye ve fermente edildiğinde 42ppm’e kadar arttırılır) [12] [13] [14] [15]
- Balık (401ppm’e kadar saptanamayacak kadar değişken) [16] [17] [18]
- Saptanabilir bir agmatin konsantrasyonuna sahip olmayan gıda ürünleri, yeşil ve kavrulmuş kahveyi, [19] unu, [20] hem soya sosuyla hem lahana suyunu içerir. [21]
Agmatin, diğer poliaminlerin yanında çeşitli gıda ürünlerinde bulunur, ancak gıdalarda bulunan konsantrasyonlar, standart ilave dozlardan önemli ölçüde düşüktür ve muhtemelen biyolojik olarak ilgili değildir.
1.2. Yapı ve Özellikleri
Agmatin, hücre zarları arasında pasif olarak taşınmasını engelleyen bir veya iki pozitif yüklü biojenik amindir . [22] Molekül normal olarak güçlü bir bazdır (alkalin), diprotonlanmış form pH 7.2’de (fizyolojik konsantrasyonların yanında) hakimdir ve en kararlı (1325kJ / mol) ve ardından monoprotonlanmış (1070kJ / mol) ve nötr 705kJ / mol) [24] ve pKa değeri 8.93’tür. [25]
- pKa değeri : Zayıf asitlerin asitliğini ifade etmek için bir indeks’tir.
Yağda çözünme özelliği ve yüksek seviyedeki hidrojen bağlarından ötürü, kötü emildiği hipotezi ileri sürülmüştür. [25
1.3. Biyosentez
[26] İnsan dokularındaki arginin dekarboksilaz (ADC ) enzim dönüşümü [26], Agmatin’in doğal olarak biriktiği bedensel alanlardan farklıdır; bu tartışmayla, çoğu bedensel Agmatin, ADC yoluyla biyosenteze bağlı olmamaktadır [27] [28] [2].
- Arginin dekarboksilaz (ADC ) :Enzimolojide, kimyasal reaksiyonu katalize eden bir enzimdir.
- mRNA : DNA’dan genetik bilgiyi gen ifadesinin protein ürünlerinin amino asit dizisini belirttikleri ribozoma taşıyan geniş bir RNA molekülü ailesidir.
Genel olarak, ADC enziminin mRNA karaciğer ve böbreklerde, iskelet kasında, ince bağırsakta, [29] [30] [31] [32] ve beyinde (hipotalamusta daha yüksek, beynin en arka kısmında saptanabilir seviyelerde bulunur) , ve hipokampus, PVN ile birlikte striatum ve beyin zarında nispeten daha düşüktür [33] Genellikle en yüksek bağışıklık doku neokortikal (beyindeki işitme ve görmeye ait bölgeye ait ) ve hipokampal internöronlarda olan nöronlarda [33]; Bazıları makrofajlar [34] ve lenfositler gibi bağışıklık hücrelerinde bulunur. [35]
- PVN : PVN, magnocellular ve parvocellular nöronlardan oluşan beyin içerisinde önemli bir bütünleştirici yerdir.
- Lenfosit : Özellikle lenfatik sistemde oluşan tek bir yuvarlak çekirdeğe sahip küçük bir lökosit (beyaz kan hücresi) şeklidir.
- Makrofaj : Bağışıklık sisteminin, hücresel enkazı, yabancı maddeleri yutup sindiren bir tür beyaz kan hücresidir. Mikroplar, kanser hücreleri ve yüzeyinde sağlıklı vücut hücrelerine özgü protein türlerine sahip olmayan diğer her şey fagositoz olarak adlandırılan bir süreçtir.
Agmatinin vücutta biriktiği yere bakıldığında, sıçan çalışmaları, en üst düzeylerin mide, ince bağırsak ve adrenal bezde olduğu gibi [27] [28] düz kas ve endotel hücrelerinde varlığı ile [36] nispeten daha düşük görüldüğünü Dalak, ana atardamar ve beyin dokusunda tespit edilen konsantrasyonlardır. [27] [28] Agmatin’de nispeten daha yüksek olan beyin bölgelerine bakıldığında, fare hipotalamik paraventriküler ve supraoptik çekirdeklerin piramitsi nöronlarla uyarıcı sinaps oluşturan nöronların terminallerinde genellikle yüksek konsantrasyonlarda [37] olduğu görülür. [38]
Alt beyin sapında , orta beyinde (ventral tegmental alan ve periakuduktal gri [39]) göreceli olarak yoğunlaşmış alanlar , Ön beyin (preoptik alan, amigdala, septum, stria terminalis yatak çekirdeği, orta hat talamus ve hipotalamus [39]) bildirilmiştir. Birkaç kaynak, sadece nöronların Agmatin sahip olmadığını ve adrenallerin [40] ve adrenal medulla’nın kromafin hücrelerinin [40] Agmatin konsantrasyonlarını ifade ettiğini ileri sürdü.
Bağırsak mikroflorası ve beslenme kaynakları da dahil olmak üzere dört diğer Agmatin kaynağı bilinmektedir. [42] Karaciğer-bağırsak dolaşımı aynı zamanda vücuttaki Agmatin konsantrasyonlarını da muhafaza edebilir. [42] [2]
1.4. Metabolizma
L-Arginin doğrudan doğruya nitrik oksite dönüşür (nitrik oksit sentezi enzimine tabi tutulduktan sonra L-sitrulin’e dönüşerek ve bir yan ürün olarak NO bırakarak), agmatin, nitrik oksit için bir madde olamaz [43] [44] ] [45] [46] Agmatin, nitrik oksit metabolizmasını etkileyebilmesine rağmen, nitrik oksit haline dönüşmesinden kaynaklanmamaktadır.
Agmatin, nitrik oksitin metabolik öncüsü değildir
Agmatin metabolizmasının olası bir yolağı, histaminin metabolizmasını işleyen ve histaminaz olarak da bilinen diamin oksidaz (DAO) enzimine [3] tabi tutulmaktadır [47] [48] ve agmatin DAO’ya tabi tutulduğunda, 4-guanidinobütirattır. [49]
- DAO :Histaminaz olarak da bilinen diamin oksidaz (DAO), hayvanlarda histamin ve putresin veya spermidin gibi diğer poliaminlerin metabolizmasında, oksidasyonunda ve inaktivasyonunda rol oynayan bir enzimdir.
Bu yol, agmatin metabolizmasında % 50’ye kadar (sıçan karaciğer gözesinde) hesaba katılması önerilmektedir [49] ve bu enzimin bastırması sıçanlarda plazma agmatini yaklaşık iki katına çıkarır (bu çalışmada 0.7 ila 1.3 μM). [47] DAO, böbrek dokusunda, sindirim sistemi ve epitel dokusunda ve endotelin düz kası hücrelerinde yüksek seviyelerde ifade edilir ancak iskelet veya kalp kası, karaciğer, beyin veya adrenallerde görülmez. [47]
Agmatin, muhtemelen agmatin’in ana kataboliti olan DAO enzimi vasıtasıyla 4-guanidinobutirat’a dönüşebilir. Bu enzim, mukus hücrelerinde , böbreklerde ve endotelde yüksek oranda ifade edildiği görülmektedir.
- Poliamin : DNA, RNA ve proteinler gibi negatif yüklü moleküller ile etkileşime giren polikatyonlardır.
Agmatin, poliamin putrescine dönüşebilir ve doğrudan üremeyi yan ürün olarak veren agmatinaz enzimi [50] [43] ile veya dolaylı olarak amonyak veren karbamoil putresine (agmatin deiminaz enzimi) dönüştürerek bunu gerçekleştirebilir Ve daha sonra putresin transkarbomilaz enzimi vasıtasıyla kendisinin (yan ürün olarak karbamoil fosfat) putresinedine dönüştürülür. [51] Yol ne olursa olsun, agmatinin yaklaşık % 10’u poliaminlere metabolize edildiği görülmektedir. [49]
Agmatin’in antizim olarak bilinen proteinin aktivitesini artırdığı kaydedildi [50], bu, poliaminlerin hücre içi birikimini [52] ve ornitin’den L-ornitin dekarboksilaz bastırması yoluyla poliamin sentezini bastırabilir; [53] bu enzim, poliaminlerin kendileri tarafından uyarılır, ve agmatin, bir poliamin olmayan bu enzimi uyaran bilinen tek moleküldür. [54]
Agmatin, arginin ve putrazin olarak bilinen poliamin arasındaki poliamin sentezinde bir ara maddedir ve agmatin’in putresine dönüşümü, idrar veya amonyak üretmek için iki yoldan birini alabilir. Buna rağmen, agmatin, hücrelerdeki poliamin miktarını azaltarak poliamin biyoaktivitesinde önleyici olabilir.
Bir Deney Ortamında çalışma ayrıca sıçan karaciğer gözesinde kuluçkalanan agmatinin yaklaşık% 1-3’ünün, poliaminlerden (% 10) ve guanidinobutiraldehitten (% 50) daha düşük olan GABA’ya [49] dönüştürüldüğünü belirtti; Agmatinin% 30’u bu çalışmada metabolize olmadı.
Muhtemelen pratik olarak alakalı değil.
Eğer ikinci yol seçilirse ve karbamoil fosfat üretilirse, aynı zamanda ADP’yi ATP’ye dönüştüren karbamat kinaz enzimi ile karbamat asit tuzuna metabolize edilebilir. Deiminaz yolağı olarak bilinen bu yol, bakterilerin arginin ve agmatin’den ATP üretmesinin bir yoludur. [55] [56] [57]
- ADP : Metabolizmada önemli bir organik bileşiktir ve canlı hücrelerde enerji akışını sağlar.
- ATP : Hücre içi biyokimyasal reaksiyonlar için gereken kimyasal enerjiyi taşıyarak vücudun enerji üretmesini sağlar.
Ornitin transkarbomilaz [58] [59] ve oksamit transkarbamilaz [60] [61], karbamat üretimi yoluyla bakteri ATP üretimiyle bağlantılı olduğu için, transkarbomilaz enzimleri (karbamoil fosfat üreten) için yukardaki mekanizma ortaktır.
Bakterilerde en az (insanla ilgisi bilinmiyor ve muhtemelen şüpheli) agmatin ATP oluşturmak için kullanılabilir.
1.5. Düzenleme
Agmatinin kan konsantrasyonları, sıçanlarda 6.8 ± 0.6ng / mL [62] ve 6.8-16.9ng / mL [63] aralığında tespit edilmiştir, ancak insanlarda 47ng / mL gibi belirgin olarak daha yüksek gibi gözükmektedir [ 64] 33.8 ± 16.6ng / mL, [65] veya 79.42-82.44ng / mL. [66]
Agmatinin sıçanlarda beyin omurilik sıvısı (CSF) konsantrasyonları 6.1-23.5 ng / mL aralığında bulunurken [63], insanlarda 24-3-54.0 ng / mL aralığındadır. [65] Son çalışma, CSF ile kan agmatin konsantrasyonları arasında olası bir ilişki olduğunu belirtti. [65]
- CSF : Beyin ve omuriliği dolduran ve çevreleyen ve şoka karşı mekanik bir bariyer oluşturan temiz, renksiz bir sıvıdır.
Sıçanlarda beyin konsantrasyonları daha yüksek (1.5-3.0nmol / g veya 0.2-0.4μg / g) iken sıçanlarda sinirsel konsantrasyonların 15.3 ± 2.4ng / g aralığında olduğu kaydedilmiştir. [67] Sığır beyindeki konsantrasyonlar, katekolaminlerinkiyle ilişkilidir, çünkü inek beyindeki 0.2-0.4μg / g agmatin, hem noradrenalin hem de dopamin için görülen 0.5μg / g konsantrasyonlara benzerdir. [67]
Agmatin’in düzenlenmiş bir kan konsantrasyonu vardır ve insanlar için sıçanlardan 50ng / mL veya daha yüksek bir aralıkta olduğu görülür. Konsantrasyonları, katekolaminlerle görülen konsantrasyonlara benzer
Metabolik sendromda plazma agmatin düzeyleri (takviyeden bağımsız olarak) önemli oranda azaldığı (% 3.7) [66] ve şizofreni [68] ve depresyonda anlamlı olarak yükselmiştir [69]
Agmatin, metabolik sendromda (az miktarda) azalmış gibi görünür ve depresyon ve şizofreni gibi bazı nörolojik bozukluklarda yükselir gibi görünür
2 Farmakoloji
2.1. Kanda Taşınması
Agmatin oral yoldan alındıktan sonra sindirildiği [70] ve oral yoldan alının biliş üzerinde etkili olduğu görülmektedir [71] (beyne ulaşabileceğini düşündürmektedir).
Dağılımı değerlendirirken, düşük dozlar (sıçanlarda 9 nmol), test edilen tüm organlarda (mide, bağırsaklar, karaciğer, dalak, akciğerler, beyin, kolon, böbrekler, adrenaller, kalp ve iskelet kası) vücuttaki konsantrasyonlarını artırabilir ve karaciğerde 3 saat sonra 64 ± 7% saptandı. [70]
Oral kullanım sonrasında emilir ve dokulara kolaylıkla dağıtılır gibi görünür; Oral yemden sonra beyne ulaşmış gibi gözüküyor.
Vücut dolaşımda agmatin’in yarılanma ömrü 10 dakikadan az gibi gözükmektedir [72] [73] ancak beyinde yarılanma ömrünün 12 saati aştığı görülmektedir [72]
Beynin yarılanma ömrü çok daha uzun gözükürken, sistemik dolaşımda yarılanma ömrü oldukça kısadır (beyinde değil)
2.2. Hücresel Alımı
Agmatin, fizyolojik pH’da protonlandığı için plazma zarlarını pasif olarak geçemez ve bu nedenle taşıyıcıları gerektirir. Sıçan Karaciğer gözesi tarafından kolayca alınır (0.37 ± 0.04 nmol / saat / mg protein oranı). [49] Putrescine’in yüksek konsantrasyonları, agmatin alımını bastırabiliceğinden [70] [74] ve tersi de, hücrelere alınma, putresin nakiliyle bir miktar örtüşme olduğu görülmektedir. [49] [74]
- Putrescine : Arginin ve ornitinin dekarboksilasyonundan kaynaklanan çürüme ile oluşan toksik bir diamindir.
- EMT : Adezyon yoluyla bağlanan polarize epitelyal hücrelerin özelliklerini yitirdiği ve bir mezenkimal hücrenin karakteristiği olan göçmen ve istilacı özellikleri kazandığı bir süreçtir.
- OCT2 : Proksimal tübül hücrelerinin bazolateral (kan) tarafında eksprese edilen başlıca böbrek alım taşıyıcısıdır. Çoğunlukla katyonik ilaçların ve dahili bileşiklerin düzeninde ve böbreklerde önemli bir rol oynar.
- OCT1 : Genlerin promotörlerini aktive eden her yerde bulunan bir DNA’dan RNA’ya genetik bilginin aktarımı yapan faktörüdür.
Ekstranöronal Monoamin Transporter (EMT) ve Organik Katyon Taşıyıcı 2 (OCT2) taşıyıcıları, benzer kapasitelerde agmatini kabul edebilir, OCT1 taşıyıcısı ise anlamlı olarak (9 kat daha az aktiftir). [22] Bu reseptörler 1-2mM’de (Km) maksimum başlangıç hızı 8-16nmol / dak / mg proteinle (OCT2 için 11.5 +/- 1.1 ve EMT için 15.9 +/- 3.5) doyabilirler. [22]
Agmatin, taşıyıcılar tarafından hücrelere ve dokuya alınmış gibi görünüyor ve kullanılan taşıyıcılar putrescine taşıyıcılarla örtüşüyor. EMT ve OCT2 nakil aracı olduğundan şüpheleniliyor
2.3. Sinirsel Dağılımı
Spesifik beyin bölgelerinde bakarken, (supplement olmadan) bazal şartlarda agmatin 22,2-25,9 (korteks (14.9-16.6ng / g), hipotalamus (19.5-23.9ng / g), beynin en arka kısmında farelerin beyinlerinde tespit edilmiştir Ng / g), serebellum (20.6-37.0ng / g) ve hipokampus (23.6-33.1ng / g). [62] Genel olarak immünohistolojik yaklaşım agmatin konsantrasyonu serebral korteks ve Subiculum (hipokampüsün alt kısmı) mevcut olduğunu, ancak bir sinirsel nakil önleyici (örneğin, ön beyin ve beyin gibi) kullanıldığında, diğer beyin bölgelerinde tespit edilebileceğini belirtmektedir; Serebellumda veya omuriliğinde saptanabilir agmatin kulplu nöron bulunmamaktadır. [39]
Beyindeki agmatin konsantrasyonları, imidazolin reseptör konsantrasyonları ile [64] ve agmatin (arginin dekarboksilaz) oluşturan enzimin konsantrasyonları ile ilişkilidir; [75] [67] agmatini (agmatinaz) bozan enzimin de hipotalamus ve hipokampusta iyi bir şekilde ifade edildiği, ancak kortekste olmadığı anlaşılmaktadır. [50]
- İmidazolin reseptör : Imidazolin reseptörlerinin son zamanlarda, kan basıncı (I-1 reseptörü) merkezi sinir sistemi kontrolünde ve serebral iskemi (I-2 reseptörü) için nöroproteksiyonda yer aldığı keşfedilmiştir.
Agmatin çeşitli beyin bölgelerinde ifade edilir ve özellikle hipokampüsün alt kısmı ve serebral kortekste zengindir.
Agmatin’in, kan beyin bariyerini geçtiği bilinmektedir; burada farelere agmatin’in 10, 50 ve 300 mg / kg’lık enjeksiyonu, en yüksek dozun sinir agmatini yaklaşık 800ng / g’ye (başlangıçtan% 700 daha yüksek) kadar arttırdığı ve enjekte edilen maymunlarda 25-200mg / kg agmatin ile beyinde agmatin (11.3μM veya 1.469ng / mL) artışının agmatin’deki plazma yükselmesinin (70.2μM veya 9.126ng / mL) yaklaşık% 16 olduğunu bulmuştur. [63] Beyinden (24-72 saat arası) oldukça uzun bir çıkış evresi var gibi gözükmektedir. [76]
Hem farelerde hem maymunlarda, L-arginin enjeksiyonları beyin agmatini arttıramadı. [63]
Agmatin, beyin agmatin konsantrasyonlarını yüksek dozlarda artırabilir ve kan beyin bariyerini geçebilir. Plazma agmatin, sinir agmatin konsantrasyonlarına göre daha büyük bir dereceye kadar yükselir ve L-arjinin verilmesi, agmatin konsantrasyonlarını arttırmaz.
3 Nöroloji
Agmatin şu anda nöronlarda düzenlenen ve bu nöronlarda presinaptik olarak depolanan metabolizmasını (hem yaratım [77] hem de yıkım [78]) sahip olduğundan nispeten yeni bir sinir ileticisi olarak düşünülmektedir; [39] [79] Sinir terminallerine nakil sonrası , [80] [81] [79] [82] Agmatin, nöronun kutupsuzlaşması üzerine serbest bırakılır ve bu da sinir ileticiler için zorunludur. [79] [82] Agmatin ayrıca beyin ve omurilikte bulunan hücreler tarafından alınabilir ve depolanabilir. [83]
Agmatin bazen bir sinir düzenleyicisi olarak da adlandırılır. Bunun muhtemelen, agmatinin düşük konsantrasyonlarda NMDA reseptörü (putrescine [84] vasıtasıyla), α2 adrenerjik reseptörler [85] ve serotonerjik reseptörler (5-HT1A / 1B) [86] aracılığıyla sinyallemeyi pozitif olarak modüle ettiği gözlemleriyle ilişkilidir; Α2 adrenerjik reseptörleri [85] rekabette bastırarak ve yüksek konsantrasyonlarda 5-HT1A / 1B sinyallemeyle zıtlık olmak üzere, poliamin bağlanma yerinde [87] (bu putrescinin [88’e bağlanarak etki yapmaktadır]) bağlanmayı bastırır.
- NMDA reseptörü : Sinaptik plastisiteyi ve hafıza fonksiyonunu kontrol etmek için NMDA reseptörü çok önemlidir.
- 5-HT1A :Santral beyin mekanizması ile kan basıncını ve kalp atım hızını azaltır, periferik damar genişlemesini uyarabilir.
- 5-HT1B : 5-HT1B reseptörleri memeli merkezi sinir sistemi boyunca ifade edilir.
- Poliamin : DNA, RNA ve proteinler gibi negatif yüklü moleküller ile etkileşime giren polikatyonlardır.
Agmatin, yeni bir sinir ileticisi madde olup, bunun nedeni, büyük miktarda mekanizma ve diğer sinir iletici sistemleri ile etkileşimlere sahip olmasıdır. Bazen bir sinir düzenleyicisi olarak da anılır; bazı mekanizmaları duruma bağlı olarak iki yönlüdür.
3.1. İmidazolin Sinir İletimi
Agmatin, imidazolin reseptörleri için I1 reseptör alt grubuna en yakın olan bir atom veya molekülüdür ve ardından I2b’dir [90] Yakınlık, α2A reseptöründen [91] klonidin yerini almasına benzer şekilde, idazoksanın reseptörden yerini alacak kadar büyüktür ve sırasıyla I1 ve I2 reseptörleri için 0.7 μM ve 1 μM’de hesaplanmıştır (EC50 değerleri). [67]
- α2A reseptörü :Norepinefrin (noradrenalin), negatif geri besleme şeklinde serbest kalmasını engelleyen damarsal kavşağın üzerinde bulunur.
- EC50 :Yarı maksimum tepki veren bir ilacın konsantrasyonudur. IC50, tepkinin (veya bağlanmanın) yarıya indirildiği bir inhibitörün konsantrasyonudur.
Agmatin, oldukça yüksek bir çekim gücüne sahip bir İmidazolin reseptör karşıtıdır. (aktivatör)
İmidazolin reseptörünün aşağı akışı, β-endorfin salgılanmasında bir artış meydana getirir. [92]
- β-endorfin : Merkezi sinir sistemi ve periferik sinir sistemi içindeki belirli nöronlarda üretilen dahili bir opioid nöropeptid ve peptit hormonudur.
İmidazolin reseptörlerinin aktivasyonu, endorfinlerin (ve bunun etkileri, muhtemelen ağrı yitimi ve kan glikozunun azaltılması) bir artışa neden olduğunu belirtir
3.2. Adrenerjik Sinir İletimi
Agmatinin adrenerjik reseptörlerin alfa-2 (α2) altkümeleri ile etkileştiği bilinmektedir ve dört alt grubun tamamına çekim gücüne sahiptir (0.8-164μM arasındaki değişken Ki [85] [67] [94] [93] ve Alfa-1 (α1) alt grubuna ya da β-adrenerjik reseptörlere anlamlı ya da zayıf bir yakınlığa sahipken, 4 μM’lik EC50’nin, adrenerjik reseptörlerin ana atom veya molekül olan 0.8 μM’da noradrenalinden düşük olduğu kaydedilmiştir [85] ] [67] Α2A reseptörlerine çekim gücü bakımından, klonidin yerini alabilir. [90] [67]
Bir çalışma, 10uM agmatinin konsantrasyon-tepki eğrisini sola kaydırdığını (noradrenalin ve agonist moksonidin sinyallerini arttıran 7,76 ve 6,86 IC50 değerlerinin göstergesi olduğunu) ve 100-1,000 μM agmatin’in karşıt etkiye sahip olduğunu ve engellediğini kaydetti ; Yazarlar, düşük dozlarda agmatinin α2A sinyallemesinin pozitif bir oynak düzenleyicisi olduğuna karar verirken, daha yüksek konsantrasyonlarda sinyallemeyi rekabetçi bir şekilde bastırdığı sonucuna varmışlardır. [85]
- IC50 :Yarım maksimum uyarıcı konsantrasyonu (IC50), bir maddenin belirli bir biyolojik veya biyokimyasal işlevi bastırma gücünün bir ölçüsüdür.
Agmatin, alfa-1 alt gruplarına veya beta-adrenerjik reseptör sınıfının tamamına yakın veya hiç çekim gücü olmayan alfa-2 adrenerjik reseptörler için yüksek çekim gücüne sahiptir. Düşük konsantrasyonlarda (reseptörü doğal olarak aktive etmeden diğer atom veya moleküllerin sinyallerini güçlendirirken) pozitif bir oynak düzenleyici gibi görünmektedir; daha yüksek konsantrasyonlarda ise, rekabetçi bir engelleyici görevi görebilir.
Deney Ortamında yapılan birçok çalışma, bu reseptörler üzerinde agmatin’in kendiliğinden karşot bir özelliği bulamamıştır (bir reseptörün sinyalleşmesinde habersiz davranmayan bir oynak düzenleyicisinin rolü ile uyumlu olarak) [95] [94] Canlı modellerde agmatinin bazı etkilerinin α2A reseptör engelleyicileri (yohimbine ve rauwolscine en sıklıkla) ile ortadan kaldırılabileceğini belirtmiştir. [96] [97]
Agmatin kesinlikle, daha önce bahsedilen oynak modifikasyona bağlı olarak, canlı modellerde α2A reseptörleri aracılığıyla sinyal vermeye başlar. Bu, muhtemelen diğer atom veya moleküllerin ortam içine dahil edilmemesi nedeniyle (agmatin diğer atom veya moleküllerin sinyalini artıracaktır, başka bir atom veya molekülün mevcut olduğunu varsaydığı için) Deney Ortamında görülememektedir
Agmatin’in konsantrasyonları sığır beyindeki katekolaminlerle (agmatin için 0.2-0.4μg / g, dopamin ve noradrenalin için 0.5μg / g) [67] ilişkiye sahiptir ve katekolamin reseptörlerinin bir alt kümesini etkilemektedir (a2 adrenerjik reseptörler) Diğerleri (α1 adrenerjik, β-adrenerjik ve dopamin D2 reseptörleri) önemli derecede etkilememektedir. [67]
Agmatin’in, monoamin oksidaz (MAO) enzimleri ile etkileştiği düşünülür; çünkü MAO enzimleri yapısal olarak imidazolin reseptörlerine benzer olduğu için genellikle imidazolin atom veya molekülleri bu özelliğe sahiptir. [99] [99] Agmatinin, flavin bölgesi yakınında MAOA için bir atom veya molekül olduğu ve başka yerlerde de 168 μM’lik bir IC50 değerine sahip olduğu, ancak önemli derecede aktif olmadığı kaydedildi. [99]:
- MAOA :Beyindeki noradrenalin, adrenalin, serotonin ve dopamin gibi nörotransmitterleri bozan bir enzimdir.
Agmatin, konsantrasyonlarının katekolamin seviyeleri ile ilişkili olması ve MAO enzimleri ile zayıf bir şekilde etkileşime girdiği bilinmektedir (MAO bastırması , muhtemelen, yüksek konsantrasyona ihtiyaç duyan ilave agmatin ilişkin pratik bir endişe değildir)
Adrenalin ve noradrenalinin, 5 μM’lik bir IC50’ye sahip adrenal kromafin hücrelerinden (bu hücreler imidazolin ifade etmekte ancak α2A reseptörlerini ifade etmemektedir [100]) konsantrasyona bağlı olarak salınması gibi pozitif düzenlemesini göstermektedir, bu nedenle bunun üzerinde etkili olduğunun bir göstergesi olduğu düşünülmektedir Katekolamin sentezini uyaran imidazolin reseptörleri [101] ve başka yerlerde, α2A reseptörlerine ikincil noradrenalin (endotel hücrelerinde) eylemlerini arttırdığı belirtilmiştir. [102]
Bu güçlendirme kokain-duyarlı (noradrenalin taşıyıcının bir engelleyici olan kokain tarafından engellenmiştir) ancak agmatin noradrenalin taşıyıcıyı hiçbir şekilde değiştirmez [102]
Bununla birlikte, endotel hücrelerinde α2A reseptörlerinin aktivasyonunun katekolamin sentezini bastırdığı gösterilmiştir [102], imidazolin reseptör aktivasyonu katekolaminleri baskılayabilir [103]
Agmetinin katekolaminler için düzenleyici bir role sahip olduğu görülmektedir ve hem salınımını başlatan hem de bastırmada rol oynamıştır. Supplement agmatin’in pratik sonuçları henüz bilinmemektedir
3.3. Glutaminerjik Sinir İletimi
Agmatin guaminin grubu NMDA reseptörleri ile etkileşime girdiğinden [105], agmatin NMDA reseptörleri için çekim gücüne sahiptir (100-300μM aralığında IC50 değeri [104]) ve hem MK-801 bağlama alanına bağlandığı belirtilmiştir [105] [106] ve poliamin bağlanma yeri (Ki 15μM) [87], ancak glutamat veya glisin bağlanma yerleri değil. [104] Agmatin, reseptörü 100uM’ye kadar aktive etme kabiliyeti taşımadığından ve MK-801 [107] gibi karşotları yerinden oynatabildiğinden, bir karşıt / engelleyicisi (fiziksel olarak glutamatı bloke etmemesi nedeniyle rekabetçi değildir).
Reseptörün bastırmasına ilişkin diğer kanıt NMDA reseptörü vasıtasıyla sinyal gönderen nörotoksik stresörlerden korumadır [108] [108] [108] [71] ancak aynı sinyal yolunda hareket edip reseptörü (kalsimisin ve staurosporin) atlatanlar etkilenmez . [108]
- MK-801 : MK-801 olarak da bilinen Dizosilpine, 1982 yılında Merck’te bir ekip tarafından keşfedilen bir glutamat reseptörü olan N-Metil-D-aspartat reseptörünün, bilişsel olmayan bir antagonistidir.
- NMDA reseptörü : Sinaptik plastisiteyi ve hafıza fonksiyonunu kontrol etmek için NMDA reseptörü çok önemlidir.
- Kainate reseptörleri : Bir iyonotropik glutamaterjik reseptör alt tipidir (AMPA ve NMDA reseptörleri ile birlikte).
- AMPA reseptörleri : Nörotransmitter glutamatın etkilerini taklit ettiği AMPA reseptörü için spesifik bir agonist olan bir bileşiktir.
Kainate ve AMPA reseptörleri çoğunlukla etkilenmez, 3.000 μM konsantrasyon sadece% 15-20 aktiviteyi bastırır [105] ve dört iki farklı üniteden oluşmuş (ε1ζ1 ila ε4ζ1) agmatin ile eşit derecede bastırılır. [104]
Agmatin’in poliamin bağlanma yerine [87] bağlanması, spermidin gibi diğer poliaminlerden gelen NMDA sinyalini, rekabetçi bastırma yoluyla reseptöre [105] sinyal göndermeden engelleyebilir. [87] Bu, aynı zamanda agmatin’in karşıt edebildiği poliamin bağlanma alanına [109] (tam olarak teyit edilmediği halde eşsiz bir yer olabilir [110]) bağladığı düşünülen histamine kadar uzanabilir. [111]
- Spermidin :Ribozomlarda ve canlı dokularda bulunan ve organizmalar içinde çeşitli metabolik fonksiyonlara sahip bir poliamin bileşiğidir.
Agmatin NMDA reseptörünün iki bölgesine bağlanır (ikisi de glutamatı bağlamaz) ve rekabetçi olmayan bir engelleyici olarak işlev görür. Poliaminlerin reseptörü aktive etmesini rekabetçi bir şekilde önleyebilir ve NMDA reseptörlerinin bastırması , diğer iki glutaminerjik reseptöre (AMPA ve kainat) kadar uzanmaz.
Bir NMDA engelleyicisi olarak agmatin’in rolü nedeniyle, glutamat doku ölümüne karşı (10-1,000 μM [108 ile zehirlenmenin % 19-51 oranında azalması] ve benzer potens ile NMDA doku ölümüne karşı koruyucu etkiler gösterir (1000μM’de% 46) [108 ].
Daha düşük konsantrasyonda agmatin (1-10μM agmatin) biyoaktif olup, katekolaminlerin glutamat doku ölümü sırasında görülen azalmayı zayıflatmaktadır [71]
1000 μM ile Deney Ortamında bu koruyucu etkiler 1.000 μM desipramin [71] ve 20μM MK-801 ile karşılaştırılabilir. [108]
NMDA’nın bastırması düşük doz agmatin’in Omurilikiçi veya 3-4. bel omurları arasındaki aralıktan enjeksiyonlarını takiben canlılarda ortaya çıkmaktadır [112] [110]
NMDA reseptörü, sinyal gönderdikleri reseptörü bloke etmesinden ötürü doku ölümüne (glutamat ve NMDA’dan) karşı snir koruyucu olarak görünmektedir. Bu, standart dozlamayı takiben canlı sistemlerde kaydedilmiştir ve maksimum potensi muhtemelen takviye ile elde edilemeyecek kadar yüksek konsantrasyonda olmasına rağmen, fizyolojik konsantrasyonlarda bile aktif olduğu görülmektedir.
Agmatinin engelleyici bir tarzda NMDA reseptörleri ile etkileşimlerinin alkol [113] [114] ve kokain bağımlılığı [115] ve NMDA reseptörü aracılı doku ölümüne karşı genel koruyucu olarak rol oynadığı düşünülmektedir. Bazı anti-depresif etkiler (nihayetinde potasyum ve kalsiyum sinyalini etkilemektedir) NMDA reseptör karşıtlığına geri dönebilir.
NMDA bastırması çoğunlukla anti-bağımlılık ve nöroprotektif özelliklerinden sonra aranır; bu arada çoğunlukla uyarıcı toksinler (aşırı glutamat veya uyarıcı kullanımı gibi)
3.4. Nitrergik Sinir İletimi
Nitrik oksit, kan dolaşımı ve kardiyovasküler sağlık ile olan etkileşiminden ötürü kardiyovasküler sağlık bölümünde daha derin incelenmiştir. Bu bölüm sadece nörolojiyi tartışıyor.
Agmatin’in, NADPH oksidaz altbiriminin aktivitesini arttırmaya ikincil olarak 29μM Ki ile nöronal bir nitrik oksit sentaz (nNOS) inaktivatörü olduğu belirtilmiştir. [116] L-Arginin’in bu alt birim aktivitesini engellemesi bilinmektedir [117] 118] ve agmatin tarafından uyarılan nNOS’un inaktivasyonunu azalttığı belirtilmiştir. [116]
- NADPH oksidaz :Hücre dışı boşluğa bakan hücreye bağlı bir enzim kompleksidir.
- nNOS : Merkezi ve periferik nöronlarda ve bazı diğer hücre tiplerinde yapısal olarak ifade edilir. Fonksiyonları, merkezi sinir sistemindeki sinaptik plastisiteyi (CNS), kan basıncının merkezi düzenlenmesini , düz kas gevşemesini ve periferik nitrerjik sinirler yoluyla damar genişlemesini içerir.
NOS engelleyicileri opioidlere toleransı zayıflatma eğilimi gösterdiği için, agmatin ve opioidlerin etkileşimlerinin altında yatan nNOS’un direkt olarak (veya NMDA aktivasyonu nNOS aktivitesinde artışa neden olduğu için dolaylı olarak dolaylı olarak inaktivasyonu) [119] [121] [122] ve NMDA engelleyicileride dahil edildi. [123] [122]
- NMDA aktivasyonu :Sinaptik plastisiteyi ve hafıza fonksiyonunu kontrol etmek için NMDA reseptörü çok önemlidir.
Agmatin, nitrik oksit sentez enziminin (nNOS) nöronal genel aktiviteleri aynı olan çeşitli formları birçok durumda, doğrudan inaktivasyon yoluyla veya bastırılan NMDA reseptörüne ikincil olarak aktivasyonunu bastırılabilir. NNOS baskılamasını içeren herhangi bir nörolojik olay için ek L-arginin olası zıttır.
3.5. Kolinerjik Sinir İletimi
1mM agmatin’in, nikotinik asetilkolin reseptörünün zıt dimetilfenilpiperazinyum (DMPP) yanıtını 67 ± 11% oranında (hem rekabetçi hem de rekabetçi olmayan bastırma belirtileri göstererek) önlediği bulunmuştur [124]
- DMPP : Otonomik ganglionlarda nikotinik reseptörleri aktive eder, ancak nöromüsküler bileşkede çok az etkiye sahiptir.
Nikotinik asetilkolin reseptörlerinin bir karşırı olabilir, ancak onaylamak için daha fazla araştırılması gerekir
3.6. Serotonerjik Sinir İletimi
PC12 nöronlarından (1-100μM) serotonin salınımını etkilemediğinden [71] ve serotonin tükendiğinde (% 70) agmatin’in antidepresan etkilerinden etkilenmediğinden, agmatin’in serotoninle çok fazla etkileşime girdiği çok fazla görünmemektedir [125] ] Agmatinin antidepresan etkileri, 5-HT1A, [89] 5-HT1B, [86] 5-HT2A, [86] [89] veya 5-HT2C [86] ‘yı bloke ettiği gibi serotonin reseptörlerine bağımlı görünmektedir ] Serotonin reseptörleri antidepresan etkileri bastırır.
- PC12 : PC12 sıçan adrenal medulla feokromositomadan türetilmiş bir hücre dizisidir
- 5-HT3 reseptörü :
5-HT3 reseptörünü bloke etmek, agmatin’in antidepresan etkilerini ortadan kaldırmaz [89], belki de bir karşıt olduğuna ilişkin olduğu için [38] [126] ve agmatin, bu karşıtlık için doğrudan bir atom veya molekülü gibi görünmemektedir. [67]
Agmatin, serotonerjik reseptör aracılığıyla sinyallemeyi arttırdığı ancak sinaptik (hücre dışı) serotonin konsantrasyonlarını değiştirdiği veya onlara gerçekten bağımlı olmadığı görülmektedir. Serotonerjik sinyallemenin bu şekilde arttırılması, antidepresan etkilerin altında yatmaktadır.
Yukarıdaki mekanizmalar ve agmatin ile serotonerjik antidepresanlar arasındaki sinerjizme bağlı olarak [127] [97] agmatinin serotonin sinyalizasyonunu arttırdığı düşünülmektedir. Bunun, reseptörün postsinaptik protein modifikasyonları ya da oynak modifikasyonundan kaynaklanıp kaynaklanmadığı bilinmemektedir (sinaptik serotonin konsantrasyonlarını etkilemesinden bağımsız görünmektedir) ve NMDA karşıtı [128] ve NOS bastırması [129] olarak bu etkilere aracılık ettiği tam olarak bilinmemektedir Hem imidazolin [130] [127] hem de α2A reseptörlerinin [97] bastırması antidepresan etkileri önlerken, serotonerjik sinyallemeyi arttırmada rol oynar.
- NOS : Nitröz olarak bilinen nitröz oksit, N-O formülüne sahip bir nitrojen oksit olan kimyasal bir bileşiktir. Oda sıcaklığında, hafif metalik kokusu ve tadı olan renksiz, yanıcı olmayan bir gazdır.
Agmatin’in serotonerjik sinyallemeyi nasıl arttırdığı belli değildir, fakat agmatin’in klasik yolaklarından biri (veya muhtemelen bunların bir kombinasyonu) aracılığıyla sinyalleme, serotonin sinyalizasyonunu yararlı şekilde değiştirir gibi görünmektedir.
3.7. Kanabirergik Sinir İletimi
Endokannabinoidler kanabinoid reseptörlerinin doğal olarak oluşan atom veya molekülleridir ve esrar kaynaklı ilk keşfedilen atom veya molekülü olan THC’den almıştır. CB1 reseptörleri, imidazolin reseptörlerinin [133] ve agmatin yerelleşmesi [28] desenine çok benzer olan orta beyindeki [131] [132] bir düzende ifade edilir ve en azından kalp dokusunda yararlı oldukları bulunmuştur . [134]
- THC : Esrarda tanımlanan en az 113 kanabinoidden biridir.
Agmatin (50-100mg / kg enjeksiyon) termal ağrı algılamasını (sıçanlarda sıcak plak testi) azaltmada etkisiz iken, 50mg / kg agmatin, iki kanabinoidergik ilacın ağrı öldürme etkisini % 300-440 oranında sinerjik olarak arttırmayı başardı. Imidazolin reseptörleri [135], CB1 karşıtları kullanıldığında da etkisi kaldırılmıştır [135]
Agmatinden agmatin takviyeli kannabinoid uyarımlı hipoterminin [136] [137] başka bir yerde görüldüğü yerlerde görülen imidazol reseptörleri ile sinyal vermenin CB1 reseptörünün etkilerini artıracağı, ancak hala bir karşıt gerektireceği ve diğer mekanizmaların oynama olasılığının düşük olduğu anlaşılmaktadır. Yohimbin sinerjiyi ortadan kaldırdığı için (α2A reseptörleri [135] hariç) NDMA karşıtlığının CB1 sinyallemesinden [138] ağrı yitimini azalttığı ve NOS bastırmasının oldukça etkisiz olduğu bilinmektedir [139] [138].
- CB1 reseptörü : Öncelikle beyin, omurilikte sinir hücreleri üzerinde bulunurlar, fakat aynı zamanda bazı periferik organlarda ve dokularda bulunurlar.
Başka yerlerde, imidazolin reseptörlerinin aktivasyonunun CB1 karşıtları SR 141716A’nın bağlanma yerinden bağlanmasını bastırıbildiğini kaydedilmiştir [140], bu, CB1 reseptörünün imidazolinin neden olduğu oynak modifikasyonu olduğunu düşündürmektedir.
- SR 141716A : Beyin kanabinoid reseptörünün güçlü ve seçici bir karşıtıdır.
İmidazolin reseptörleri aracılığıyla sinyal göndererek, agmatin, kanabinoidlerin ısıya karşı ağrı öldürme etkilerini arttırdığı görülmektedir. İkisi arasında genel bir sinerji söz konusudur ve agmatinin rolü, CB1 reseptörlerinin dolaylı bir pozitif düzenleyicisi (muhtemelen reseptörün yapısını değiştirerek sinyal vermeyi teşvik eder) gibi gözükmektedir.
Esrar olarak bilinen böyle sinirsel ağrıların giderilmesi için potansiyel keşfedilmemiş sinerjidir.
3.8. Opioidergik Sinir İletimi
Adrenal bezlerde imidazolin reseptörlerinin (özellikle I2 reseptörlerinin) aktivasyonu, merkezi ve organ etkileri olan β-endorfinin (doğal olarak üretilen bir opioidergik ağrı kesici) [92] salınmasına neden olduğu görülmektedir.
Toleransın önlenmesinin imidazolin reseptörlerinin aktivasyonuna bağlı olduğunu bildiren bir çalışma olmasına rağmen, Opioidergik acı yitimi [123] ve tolerans gelişiminin zayıflaması [141] daha önce NMDA karşıtları ile (muhtemel Agmatin rolü) kaydedilmiştir [142]
Agmatin, adrenal bezlerde imidazolin reseptörlerini aktive ederek doğal olarak bazı opioidleri salabilir. Agmatinin opioidlerle nasıl etkileşime girdiğine ilişkin aşağıdaki bilgiler (β-endorfin için de geçerlidir) açısından, işleyen adrenalardaki kişilerde kendisiyle biraz sinerjiktir.
Α2A reseptörlerinin [144] aracılık ettiği ve oksikodona [145] ve fentanil’e (morfinine benzer iki opioidergik ilaç olan) uzanan görünen agmatin [143] birlikte uygulandığında morfinin kısa süreli analjezik (ağrı kesici) etkileri artar.
Kısa süreli acı yitimi için, agmatin, opioidlerle sinerjik görünmektedir
Agmatin kuvvetli -opioid için 4nmol 3-4. bel omurları arasındaki aralıktan enjeksiyon ile karşıtları toleransı bastırdığı tespit edilmiştir [112], tek bir doz, 48 saate kadar etkili olduğu görünür. [112] Oral agmatin (40-80 mg / kg) verilen rhesus maymunlarında da belirtilmiştir. [146]
Araştırma hayvanlarında opioidergik ilaçlara karşı toleransın azaldığı belirtilmiştir. [143] [120]
Opioidlere tolerans (uzun süreli kullanımla birlikte verilen etkinliğin azaltılması) agmatin birlikte uygulandığında zayıflamış görünmektedir ve bu da opioidlerin acı yitimi etkilerini sinerjik olarak muhafaza eder
Adrenerjik reseptörler a2a reseptörü [147] [148] ve β-adrenerjik reseptörler, morfin çekilme semptomları hafifletmek mümkün bastırma aktivasyonu ile, opioid reseptörleri ile ilgili olan, [149] tersine, (a2a engelleyicisi) yohimbin negatif geri çekme semptomları artırmaktadır . [150] [151]
Bağımlılık yapıcı özellikleri (kendi kendine uygulama genellikle incelenmiştir) ya da opioderjik ilaçların yoksunluk belirtileri ölçmek çalışmalarda agmatin fentanil kendi kendilerine uygulamalarına azaltmak için not edilmiştir. [152] [153]
Koşullandırılmış yer tercihi ile ilgili olarak (CPP; başka bir düşünce üzerinden bir yer için bir tercih bağımlılık hareketinin bir biyolojik olarak [154]), morfin ile agmatin yapılan birlikte işlem esnasında, morfin kaynaklı koşullandırılmış yer tercihi artırmak için mümkün olduğu [155].
Agmatin, morfin veya fentanil gibi opioid ilaçlarla sinerjik görünmekte, toleransını önlemekte ve muhtemelen bunun bağımlılık potansiyelini azaltmaktadır. Agmatin’in bu etki üzerinde oldukça güçlü olduğu görülüyor.
3.9. Ağrı Ve Ağrı Yitimi
Agmatin genellikle asidite (protonlar) tarafından aktive edilen altı asit algılayan iyon kanalından [158], ASIC3 için [156] [157] bir proton olmayan atom veya molekülü gibi görünmektedir; [159] ASIC3, kolayca desensitize olmadığı için biraz eşsizdir [160] [161] ve aktivasyonun ağrı algısıyla ilişkili olduğu duyusal nöronlarda bulunur [162] [163]
- ASIC3 : Memelilerde trimerik asit algılayıcı iyon kanalları oluşturan proteinleri kodlayan beş paralog genden biridir.
Agmatin, nötr pH’da sinyal vermeye (7.4) neden olabilir ve protonların kanal üzerinde yaptığı yere bağlanmadığı için (asit algılaması sırasında) bir proton-dışı atom veya molekül olarak sınıflandırılır. [157] Bu aktivasyon, agmatin’e (poliaminler veya arginin ile birlikte görülmemiştir) özgündür ve agmatin’in aynı zamanda reseptörleri asiditeye duyarlı olduğu bulunmuştur (pH 7.0). [157]
Bununla birlikte, yazarlar, düşük konsantrasyonda agmatin ile eşleştirilmiş düşük potensli sinyallemenin, ASIC3’e bağımlı vasıtalarla farelerde agmatin ile uyarılabilmesine rağmen normal koşullar altında önemli bir endişe olmadığı anlamına gelebilir [157]. ]
Agmatinin yükseldiği (algılanan ağrı artışı ile birlikte) kansere ve travma hastalarına asit iltihaplı ağrı ile ilgili olan koşullar (kan pH’sı yaklaşık 7.0) iltihaplanmayı, enfeksiyonu, aiırı zayıflığı , kan toplağı ve egzersizini içerir [158] 164] [34]
Agmatin, asidite bağlı ağrı bulgulamasında rol oynayan ASIC3 reseptörünü aktive edebilir ve bu mekanizma ile teorik olarak ağrıya neden olur. Bu yolağın pratik önemi bilinmemektedir, ancak şu anda zaman agmatinin normalde ağrı sinyali vermediği, ancak normalde yüksek konsantrasyonların, asit kaynaklı ağrı arttırabileceği akla yatkındır
Bir asetik asit kıvrılma testinde (karın ağrı modeli), agmatin zayıf acı yitimi özelliklere sahiptir. [142] İltihaplı veya nöropatik ağrı testlerinde agmatin, doza bağımlı ağrı azalması üretir. [165] [166]
Agmatin tek başına ya ağrı kesici etki göstermedi [135] veya sıçanlarda kısa süreli bir aktiviteye (10-30 dakika, sadece termal Ağrıya aşırı duyarlı olmaya karşı) sahip olduğu bulundu. [72] Kısa süreli etkiler agmatin’in kısa yarılanma ömrü (10 dakikadan az [72]) ve adrenal bezlerden β-endorfinin salınımı ile ilişkili olabilir. [92]
Agmatin, ısı ağrısına karşı etkili gözükmemekte ve karın ağrısına karşı oldukça zayıf görünmektedir. Buna rağmen, agmatin’in iltihapşı ve nöropatik ağrı üzerinde doz bağımlı ağrı giderme özelliklerine sahip olduğu görülmektedir.
Radikülopati (bacağa giden bir sinirin ezilmesi sonucu ağrının ortaya çıkması) ile ilişkili dejeneratif omur hastalığı (n = 61) olan hastalarda 2.67g Agmatin Sülfatın 14 gün süreyle kullanıldığı (patent sahipleri tarafından kısmen Trimarco Tıp Bölümü tarafından finanse edilen) bir çift kör çalışma, 14 gün sonra azalma olduğunu bildirdi Ağrıda VAS değerlendirme ölçeği , McGill ağrı anketi ile değerlendirildi, ancak Oswestry Özürlülük Endeksi üzerinde anlamlı bir iyileşme yoktu. [167] Agmatin sülfatın 60-65 gün süreyle kesilmesinin ardından bu faydalar hala istatistiksel olarak anlamlı olarak göründü. [167]
- VAS : Bir değerler sürekliliği boyunca aralıklı olduğuna inanılan ve kolayca doğrudan ölçülemeyen bir karakteristiği veya tutumu ölçmeye çalışan bir ölçüm aracıdır.
- McGill ağrı anketi : McGill Ağrı Anketi bir kişiyi değerlendirmek için kullanılabilir.
- Oswestry Özürlülük Endeksi : Bel ağrısının engelliliğini ölçmek için bir testtir.
Tecrit halinde agmatin, bu belirli hastalık halindeki ağrı algısını azaltmada etkili gibi görünmektedir ve ağrı azaltma derecesi dikkate değer olduğu için daha fazla araştırma gerektirmektedir.
3.10. Bağımlılık
Α2A reseptörleri, aktivasyonun bağımlılık için yararlı olduğu düşünülen bağımlılık için merkezi bir noktadır (bağımlılık için klonidin ve nikotin bağımlılığı [168] [169] ile görüldüğü gibi) ve bastırması bağımlılığın olumsuz bir etkisi olduğu düşünülmektedir (bazıları Bağımlılık yapıcı bir tarzda hareket eden sınırlı yohimbine kanıtıdır).
Α2A reseptörleri, uyarımı (sıçanlarda hareketle değerlendirilir) arttıran nikotin [170] gibi bağımlılık yapan ilaçlara yanıt olarak yukarı doğru düzenlenir ve sonraki dozlarda tek bir doza göre bağımlılıktır. [171] Bu yükseltmenin önlenmesinin şu anda agmatin’in nikotinle uyarılan koşullu aşırı yer değiştirme [172] önlediği mekanizma olduğu ve bir haftalık kronik dozlamanın görüldüğü yerde hareketliliğin arttığı varsayılmaktadır [171]
Agmatin, muhtemelen α2A reseptörlerinin yükseltilmesi (nikotinin tekrarlanan dozlarla daha fazla katekolamin salınmasını önlediği) önlemekten kaynaklanan kronik nikotin alımıyla aşırı yer değiştirme artışını önler gibi görünüyor.
Yaşlı insanlarda sallanma / titreme [173] ve anksiyete [174] gibi alkol yoksunluğu semptomları, agmatin verilmesi ile zayıflatılır. Bunun mekanizması henüz bilinmemekle birlikte, NMDA reseptör karşıtı ile ilişkili olduğu düşünülmektedir, çünkü poliaminlerin, alkolden çekilme sırasında NDMA reseptörünü nörotoksik bir tarzda aktive ettiği bilinmektedir [175] [176] ve agmatin, yerleşmiş bir engelleyicisidir .
Alkolün geri çekilmesi sırasında yararlı olabilir ve nikotin ve opioidlerin α2A reseptör upregülasyonuyla ilişkili olmasına rağmen, alkolle olan etkileşimler muhtemelen başka bir mekanizma (NMDA karşıtı ) tarafından aracılık edilir
Kokain bağımlılığının, Deney Ortamında NMDA bastırması [insanlarda o kadar umut verici bulgu olmaksızın [177] [178] tarafından desteklendiği ve planaryalarda ( çok küçük bir kurtçuk çeşiti) NOS bastırması (memeli benzeri sinir iletimine sahip hayvanların memeli olmayan modeli) , [179] ki bunlar kokain bağımlılığı ve agmatin arasındaki şu anda varsayılan hipotez bağlantılarıdır.
Agmatin’in, fentanilin yol açtığı bağımlılık davranışını önlemek için yeterli bir dozda birlikte uygulanması, sıçanlarda kokainle ilişkili bağımlılık davranışını değiştirmeyi başaramamıştır. [153] Bu verilerin pratik önemi bilinmemektedir çünkü kokain farelere aşırı derecede bağımlılık yapmaz ve ödül durumu yoğun tatlılığa göre daha düşüktür [180] [181] Halen insanlarda kanıt bulunmamaktadır.
Kokain üzerindeki anti-bağımlılık özelliklerine ilişkin kanıtlar, sıçan modellerinde sınırlıdır ve fazla umut verici değildir, ancak bu konuda sıçanlar ve insanlar arasındaki bilinen tür farklarından dolayı agmatin’in pratik olarak kokain bağımlılığını nasıl etkileyeceği belirsizdir
3.11. İnme ve Kansızlık
Genel olarak, deneysel olarak uyarılan inme öncesinde agmatin ile ön işleme tabi tutulan araştırma hayvanları, yaklaşık 100 mg / kg enjeksiyonlarla nörokoruma göstermektedir. [182] [184] [185] [186] [187] [184] [184] [184]
Genel olarak, deneysel olarak uyarılan inmeden önce agmatin ön-tedavi edilmesi, araştırma hayvanlarında oldukça sinir koruyucudur ve aynı zamanda oldukça güvenilirdir.
Agmatin’in bastırdığı , inmeleri diferansiyel modüle ettiği nitrik oksit sentezi (NOS) enzimleri, eNOS’un damar genişlemesi yoluyla koruyucu olduğu hallerde iNOS aşırı nitrik oksit üretimine ve hasar görmesine neden olur [188] [189]; nNOS da bir nörotoksik [191]) ve iNOS’a karşı bastırması (220μM), eNOS’un (7500μM) [116] 34 kat daha güçlü olduğu için inme önlemesinde agmatin’in hedeflerinden biri olduğu düşünülmektedir.
İnme sonrasında NOS enzim içeriğindeki tipik değişikliklerin (iNOS’da artış ve eNOS’lu kısa süreli baskılama) agmatin ön tedavisi ile zayıfladığını, iNOS% 13.35 (6 saat) ve% 46.30 (24 saat) [192] azaldığını ve normalizasyona uğradığını belirtti 4 gün içinde görülür. [182]
- NOS : Nitröz olarak bilinen nitröz oksit, N-O formülüne sahip bir nitrojen oksit olan kimyasal bir bileşiktir. Oda sıcaklığında, hafif metalik kokusu ve tadı olan renksiz, yanıcı olmayan bir gazdır.
- eNOS :İnsanlarda kromozom 7’nin 7q35-7q36 bölgesinde yer alan NOS3 geni tarafından kodlanan bir enzimdir.
- iNOS : İltihaplanma koşullarında ortaya çıkar ve büyük miktarlarda Nitrik oksit üretir
Nitrik oksitin azaltılmış iNOS üretimine ikincil (doğrulanmış), [187] peroksinitrat konsantrasyonlarında bir azalma da tespit edilmiştir. [183]
İNOS’daki proinflamatuar değişikliklerin azaldığı ve eNOS’un koruyucu etkilerinin korunduğu agmatin takviyesine cevaben nitrik oksit metabolizmasında faydalı bir modülasyon var gibi görünüyor. Bu, nitrik oksit ve peroksinitrat seviyelerini düşürür, bu inme sırasında anormal yükselmeler zararlıdır
Aquapolin-4 reseptörü, beyin ve omurilikte bulunan hücrelerde belirgin olarak su emen beyin ve omurilikte bulunan hücrelerde reseptördür [193] ve bu reseptörün azaltılması (veya ortadan kaldırılması) beyin ödeminde sağkalımı artıran [194], kansızlık inmesinden sonra uyarılır. [195] Agmatin (100 mg / kg), deneysel inme sırasında görülen artmış aquaporin-4 dönüşümünü zayıflattığı ve muhtemelen inmeden çıkan beyin ödemine ikincil olarak nitelendirildiğini belirtti. [182] [184]
- Aquapolin-4 reseptörü : AQP4, hücre zarından su geçiren entegre hücre proteinlerinin aquaporin ailesine aittir.
Agmatin ön-tedavisi ile aquaporin-4 dönüşümü belirgin şekilde azalır ve canlılarda inme sonrasında bu daha az ödem oluşur. Bu muhtemelen başka bir hedefe ikincil olan agmatin’in bir etkisidir.
Nöronlara ve işlevsiz sinir hücrelere bakıldığında, beyin ve omurilikte bulunan hücreler (glial hücre), canlılarda [196] [182] ve izole edilmiş hücrelerde (100uM) 100mg / kg enjeksiyonlarında agmatin ön tedavisi ile korunmuş gibi görünmektedir. [185]
Labaoatuar çalışmada hücresel koruyucu bir etki olan IκBα ve IKKα / β’nın daha fazla aktivasyonu ile ilişkili çekirdeğin NF-kB yer değiştirmesini arttığı doğrulandı [185]. [197] Agmatinin başka yerde [198] [199] PI3K / Akt aktive ettiği ve bunun hücresel bir sağkalım yolu olduğu bilinmektedir (Akt, NF-kB yoluyla survivin’e sinyal verir). [200] [201] [202]
- IκBα : NF-KB transkripsiyon faktörünü bastırma işlevi gören hücresel proteinlerin bir ailesinin bir üyesidir.
- NF-kB :DNA’dan RNA’ya genetik bilginin aktarımını, sitokin üretimini ve hücre sağkalımını kontrol eden bir protein kompleksidir.
- PI3K : Hücre içi kalsiyum konsantrasyonlarındaki artışlar ve tehdit durumunda sırasında ortaya çıktığı bilinen Ras, 231’in kalsiyuma bağlı uyarımı ile aktive edilir.
- Akt : Kas protein sentezini tetiklemek üzere aktive olan proteinler
- Survivin :Kaspaz aktivitesini engelleyen bir protein
Agmatin, hücreleri kansızlık/ hipoksik ölümden koruduğu görülmektedir; bu, NF-kB’nin artan aktivitesinden kaynaklanıyor ve bu da kalkanı artırıyor
3.12. Stres ve Kaygı
Arginin dekarboksilaz enziminin her iki bitkide [203] ve bakterilerde [204] asitlik ile uyardığı (aktivitede arttığı) ve ozmotik [205] ve bakır kaynaklı oksidatif strese karşı duyarlı olduğu gösterilmiştir [206]
- Arginin dekarboksilaz enzimi : Enzimolojide, kimyasal reaksiyonu katalize eden bir enzimdir.
Yukarıdakilere ve soğuk strese maruz kalan memelilerde beyin (15.3 ± 2.4ng / g ila 57.4 ± 19.6ng / g;% 275 [62]) ve plazmada (6.8 + 2.4ng / -0.6ng / mL ila 58.1 +/- 12.8ng / mL;% 754 [62]) agmatin görüldüğünde, arginin dekarboksilaz enziminin strese duyarlı olduğu ve stres dönemlerinde agmatini arttırdığı görülmektedir (ancak en az bir çalışmadan Agmatin’de plazma artışının enzim üzerinde nedensellik göstermesi çok hızlı olabileceği 4 saat içinde tespit edildiği için kağıtta diğer mekanizmaların bulunabileceği ileri sürülmektedir [62].
Arginin’den agmatin üreten enzim (arginin dekarboksilaz olarak bilinir), stres dönemlerinde artmaktadır ve bu nedenle stres tepkisi, agmatin’de büyük bir artış ile karşılanmaktadır. Bunun, strese karşı koruyucu bir cevap olduğu düşünülmektedir.
Kanda oksijenin azalması sırasında arginin dekarboksilaz aktivitesinde bir artış kaydedilmiştir. [187]
Mekanik olarak, 3-4. bel omurları arasındaki aralıktan agmatin (10-40 mcg) infüzyonu, lokus coeruleus’taki (beynin noradrenalin deposu olarak bilinen bölgesi) nöronların ateşlenmesinde konsantrasyona bağlı artışlara neden olabilir (nitrik oksit sinyallemesi yoluyla [207]). Bu beyin bölgesi, özellikle anksiyete ve depresyona, strese vücut yanıtında rol oynamaktadır [208] ve bu nedenle agmatin’in eylemleriyle ilişkili olduğu düşünülmektedir.
Alkolle yapılan birkaç endişe, alkolden kaynaklanan kaygının ortadan kalkması ve alkolün sebep olduğu kaygı aslında agmatin bağlıdır (tükenmekte olan agmatinin oluşumunu engeller). [174]
Agmatin, beyinde anksiyete işleme ile ilgilidir ve alkol, agmatin konsantrasyonlarını etkilemek yoluyla endişeyi azaltır gibi görünmektedir.
Agmatin [209] ve 40 mg / kg [210] ‘un 20-40 mg / kg enjeksiyonları, artmış bir labirent plus testi (EPM, sıçanlar için standart anksiyete testi) kullanan çalışmalarda, kaygı düzeyini karşılaştırılabilir (önemsiz derecede daha güçlü) etkilere göre azaltırken etkinlik göstermektedir . [210] Agmatinin oral alımını (10-40mg / kg) alan bir çalışmada, sıçanlarda sosyal bir çatışma testinde endişe düzeyinin diazepam ile kıyaslandığında azaldığı; 80mg / kg’dan 5mg / kg’a kadar etkili olmadığı belirtildi. [211]
- EPM : Endişe benzeri davranışı ölçmek için en çok kullanılan testlerden biridir.
Açık renk karanlık kaygısı testinde, benzer dozlarda agmatin farelerde etkili olmamıştır [125] veya sadece farelerde veya 10 mg / kg oral alımda 80 mg / kg enjeksiyonda dikkate değerdir; Her ikisi de referans ilaçtan (diazepam) daha az güçlüdür. [211]
100mg / kg’ın hiçbir etkisi olmamış [210] veya kaygı düzeyini gerçekten kötüleştirdiği bulunmuştur [209]
Agmatin, depresyonun azaldığı yere benzer bir dozda kaygıyı azaltabilir görünmesine rağmen, agmatin ile gösterilebilir bir çan eğrisi ve dozun iki katı endişe giderici etkilere sahip değildir. Maksimum etkinlikte toplam endişe giderici etki referans ilaçlardan daha düşük veya karşılaştırılabilir.
3.13. Depresyon
Agmatin kinetiklerinin (takviyesiz) depresyonu olan kişilerde daha yüksek kan konsantrasyonları [69] olduğu gibi depresyonu olan kişilerde de değiştiği görülmektedir, aynı zamanda hem depresif hem de bipolar kişilerde agmatinaz aktivitesi ile değerlendirildiğinde daha yüksek bir bozulma vardır. [33] Agmatin, bupropion (Wellbutrin) [69] tarafından konsantrasyonda azalma ile birlikte farmasötik depresanlardan etkilenirken SSRI ilaçları agmatin konsantrasyonlarını arttırır. [127] Depresyonun, imidazolin reseptör sinyali ile ilişkilendirildiği görülmektedir. [212]
- SSRI :En yaygın antidepresanlar seçici serotonin geri alım inhibitörleri (SSRI) olarak adlandırılır.
Depresyon, değişebilir agmatin kinetiği ve fonksiyonuyla ilişkilidir, ancak gerçekten tahmin edilebilir bir şekilde değildir. İlaç anti-depresanlarının hem depresyonu tedavi edebilmelerine rağmen hem agmatinde farklı etkileri olduğu görülmektedir (azalan veya artmaktadır)
Agmatin, kendiliğinden kullanıldığında, başka yerlerde 5-40 mg / kg ile teyit edilmiş olan, oral yoldan alınan 10-40 mg / kg (insan eşdeğeri 1.6-6.4 mg / kg) zorunlu yüzme testinde hareketsizlik süresini azalttığı görülmektedir [ 89] veya 10 mg / kg oral alım [71] ve çeşitli dozlarda enjeksiyonlar (0.01 ila 100 mg / kg arasında herhangi bir yerde; 10-50 mg / kg aralığında daha fazla etkinlik ile). [97] [210] [125] Aktif kontrolleri kullanan çalışmalarda, agmatin (50 mg / kg), 15 mg / kg imipraminden [125] veya 10-100 mg / kg’dan az etkili olup, hepsi de 30 mg / kg imipramine karşılaştırabilir. [210]
Tail süspansiyon testlerinde antidepresan etkileri de bildirilmiştir [71] [97] ve 40-80 mg / kg oral yoldan 10 mg / kg imipramine benzer etki göstermekteydi. [71]
- Tail süspansiyon testi : Potansiyel antidepresan ilaçların taranmasında faydalı bir fare davranış testidir.
Agmatin’in kendiliğinden, orta dozajlarla antidepresan etkilere sahip olduğu ve bu antidepresan etkilerin sıçanlara oral yoldan verilmesinin ardından doğrulandığı kaydedildi. Potansiyel, referans ilaç olan imipramine kıyasla daha düşük veya zayıf görünüyor, ancak ikisi arasındaki karşılaştırmalar tutarlı değil. 10-40 mg / kg sıçanlar için tahmin edilen insan dozu 1.6-6.4 mg / kg’dır (70 kg kişi için 217-435 mg)
Agmatin’in başka yerlerde de bir başarısızlık kaydedilmesine rağmen, bupropion (imidazolin reseptörlerine bağımlı 10-20 mg / kg agmatin enjeksiyonlarında [130], imipramin (0.01-50 mg / kg) [97] gibi sayısız antidepresanlarla sinerjik olarak çalıştığı bulunmuştur [127 ]], SSRI’lar (imidazolin reseptörlerine bağlı olarak 5-10 mg / kg agmatin enjeksiyonu) [127] ve garip bir şekilde putresin (bir poliamin) depresif semptomlarda agmatin ile sinerjiktir (0.001 mg / kg agmatin enjeksiyonu). [84]
[97] [97] [97] [97] Yohimbine (α2A reseptör blokeri), [89] [97] [97] ve GMP kendisinin antidepresan etkileri ortadan kaldırıldı [97], potasyum kanal engelleyicilerinin Agmatin çalışmalarının, Viagra gibi PDE5 engelleyicileri tarafından bastırılabilen mekanizması olmaktır. [213] 5-HT1A, [89] 5-HT1B, [86] 5-HT2A, [86] [89] veya 5-HT2C [86] serotonin reseptörlerini bloke etmek, opioid reseptörlerinin delta ve mu alt birimlerini bloke eden etkileri bloke eder [214] ve potasyum kanallarının açılması agmatin’in etkilerini önlediği görülmektedir [215]
Prazosin (bir α1A reseptör bloke edici), [97] serotonin tükenmesi, [125] beta-adrenerjik sistemi (propanolol), [86] [89] veya 5-HT3 reseptörlerini bloke eden etkiler etkilenmez. [89]
Potasyum kanallarının bastırması , daha önce bahsedilen klasik antidepresanların adenosin (dahili sinir iletici ) [220] gibi potasyum kanallarını [216] [217] [218] [219] [219] bastırma yeteneğine sahip oldukları için sinerjizmin altında yatabilir. Folik asit [221] potasyum kanallarını bastırmada pro-depresan bir etki gibi görünmektedir [222] [223] Daha önce, çeşitli serotonin reseptörlerinin engellenmesinin sinerjiyi bastırdığı ve serotoninin muhtemelen reseptörü aracılığıyla potasyum kanallarına aracılık ettiği belirtildi. [224]
Son olarak, agmatinin kendiliğinden 500μM [225] potasyum kanallarını bastırmasına rağmen [225] potasyum kanalı bastırıcılarıyla antidepresan etkileri ortadan kalkar [215]
Agmatin’in anti-depresan etkileri, diğer maddeleri arttırarak ortaya çıkmaktadır. Agmatin potasyum kanallarını kendisi engelleyemezken, (başka şekilde) diğer maddelerin potasyum kanallarını bastırma kabiliyetlerini artırır ve antidepresan etkilerine katkıda bulunur. Bu sinerjizm, serotonin reseptörleri yoluyla sinyallemenin (aktif moleküllerin muhtemelen sinyal vereceği) korunmasını ve α2A reseptörleri vasıtasıyla sinyalleşmenin korunmasını gerektirir (agmatin muhtemelen sinyal gönderir)
Depresyon (majör depresif bozukluk ve unipolar / bipolar ayrımlar) olan ve antidepresan direnci olmayan insanlar üzerinde yapılan ve bir başka farmasötik ilaç olmaksızın oral olarak 2-3 g agmatin verilen bir pilot çalışma, üç test edilen deneklerin hepsinin depresyonun hafifletildiğini bildirdikleri [226] [226], hayvan çalışmalarına [125] benzer şekilde, agmatin’in antidepresif etkilerinin serotonin ile ilgisi olmadığını öne sürerek, PCPA uygulaması ile tersine çevrilmemiştir.
Çok küçük bir pilot çalışma, agmatin’in depresyonun hafifletilmesini (yani, iyileştirici bir etki)
3.14. Gıda Alımı
Nöropeptid Y, açlığı pozitif olarak düzenleyen ve bunun bir ‘orexigenic’ (açlık arttıran veya iştah uyaran) hormonu [227] olarak bilinen ve hipotalamusun paraventriküler çekirdeğine (PVN) enjeksiyonu ile besin alımına neden olan bir peptid nevrohormondur. 228] Nöropeptid Y, α2-adrenerjik reseptörlerle yüksek oranda ilişkilidir [229] [230] [231] ve aktivasyonu (genellikle klonidin yoluyla çalışmalarda) NPY konsantrasyonlarını arttırır [232] [233] Bu nedenle karşıtların (yohimbine ve rauwolscine ) iştahı bastırır. [234] [235]
- PVN : Magnocellular ve parvocellular nöronlardan oluşan beyin içerisinde önemli bir bütünleştirici yerdir.
- Nöropeptid Y : Hem merkezi hem de periferik sinir sistemlerinde çeşitli fizyolojik ve homeostatik süreçlere katılan 36 amino asitli bir nöropeptiddir.
Agmatin verilmesinin doymuş sıçanlarda besin alımını artırdığı gösterilmiş ancak aç fareler [236] ve agmatin’in hipotalamusa verilmesi, artan nöropeptid ile ilişkili olarak gıda alımı artışına (24 saatte% 10-20 nmol neden olur) ve artmış nöropeptide Y aktivitesine neden olur , [96] α2-adrenerjik aktivasyonun aracılık ettiği düşünülmektedir, çünkü yohimbin etkileri zayıflatmıştır. [96] Agmatinin karıniçi enjeksiyonu (40-80 mg / kg) aynı zamanda gıdaların alımını arttırmada (24 saat içinde% 44-49) etkili olurken, 20 mg / kg etkisizdi. [96]
Agmatin, yohimbin’e zıttır ve α2A reseptörleri aracılığıyla agmatin infüzyonları iştahını artırabilir, ancak sadece aç farelerden ziyade ‘yok’ farelerde bulunur. Bu bilginin pratik önemi bilinmemekle birlikte, yeterince yemek yiyememeleri nedeniyle kilo alamayan insanlar için umut vericidir
3.15. Hafıza ve Biliş
Agminatin, hipokampusta, özellikle CA1 piramital nöronlarda yüksek seviyelerde depolandığı bilinmektedir. [38] Sinaptik Ca2 + ‘ya bağımlı ekzositotik süreç [238] yoluyla glutamat kesecikler [237] [64] ile birlikte serbest bırakıldığı düşünülmektedir [238] ve hipokampal aksiyon potansiyelleri (nöronal aktivasyon) [238] ile birlikte sinir kavşağındaki agmatin seviyeleri artmaktadır.
Öğrenme süreci (sıçanlarda su labirenti testinde % 60-85); [239] [237] [240] [239] ve yüksek artışlar (% 210-573) ancak 85-95 dakika rapor edilmiş olmasına rağmen [241] ] bazal agmatin arttığı görülüyor, ancak daha düşük aralıktatır. [241] Agmatin, müteakip hipokampal deşarjları hafifletir [242]
- CA1 : Alyuvarlarda en yüksek seviyede bulunan sitosolik bir proteini kodlar.
- Ekzositotik süreç : Eksositoz, bir hücrenin salgı ürünlerini sitoplazma yoluyla plazma hücresine taşıdığı bir süreçtir.
- Hipokampal : Hipokampal oluşum, beynin medial temporal lobunda bir bileşik yapıdır.
Agmatin’in öğrenme sürecinde stratum radiatum ve ön ve perirhinal kortekslerde (bilgi depolanmasında önemli bir rol oynayan beyin bölümü) [243] yükseldiği, agmatin infüzyonları ile nöronal aktivitenin arttığı locus coeruleus (beynin noradrenalin deposu olarak bilinen bölgesi) [39] da yükseldiği saptanmıştır [207] [244] ön korteks, davranışsal öğrenme ve yürütme işlevinde [245] [246] yer alır ve perirhinal korteks (hem de hipokampus), yerinden edilmiş nesne tanımayı olumlu yönde etkiler [244] . [247]
Agmatin’in bir sinir iletici rolü hafıza oluşumunda yer alır. Öğrenme görevleri sırasında, agmatin, hipokampus, prefrontal korteks, katman radiatum ve perirhinal kortekste yükselir ve glutamat ile ilişkili olan glutaminerjik sinyalizasyonun negatif düzenleyicisi gibi görünmektedir (NMDA reseptör karşıtlığı muhtemelen burada da yer almaktadır)
- NMDA reseptörü : Sinaptik plastisiteyi ve hafıza fonksiyonunu kontrol etmek için NMDA reseptörü çok önemlidir.
Bir çalışma (nöronlardan ziyade insan mezenkimal kök hücrelerde de olsa), arginin dekarboksilaz enziminin artan aktivitesinin, BNDF ikincil olduğunda görülen artışa neden olduğu düşünülen agmatinde (2 kat) bir artışa neden olabileceğini kaydetti ve buda Akt ve CREB’in fosforilasyonuna kadar uzanır. [198] BNDF, agmatin’in aktive olduğu Akt’in [249] aşağı düzenlenmesinde CREB’nin [248] akış aşağısındadır; [199] bu yol bu kök hücrelerde prosurvival olarak görülür, fakat nöronlarda sinaptik plastisite ve hafıza oluşumunu pozitif olarak düzenler. [251]
- Mezenkimal kök hücresi : Osteoblastlar (kemik hücreleri), kondrositler (kıkırdak hücreleri), miyositler (kas hücreleri) ve adipositler (ilik yağ dokusuna yol açan yağ hücreleri) dahil olmak üzere çeşitli hücre tiplerine farklılaşabilen çok hücreli stromal hücrelerdir.
- BNDF :Kanonik sinir büyüme faktörü ile ilişkili olan nörotrofin büyüme faktörleri ailesinin bir üyesidir. Beyinde ve çevredeki nörotrofik faktörler bulunur.
- Akt : Kas protein sentezini tetiklemek üzere aktive olan proteinler
- CREB : Nöronlardaki CREB proteinlerinin uzun süreli hafızaların oluşumunda rol oynadığı düşünülmektedir.
BDNF’deki muhtemel artışın (hafıza oluşumunda rol oynayacak) ötesinde, 2 haftalık 20mg / kg agmatin alımının prefrontal kortekste artmış adenilat siklaz aktivitesi vardır. [89]
Agmatinin, artan sinaptik oluşuma ya da cAMP aktivitesini arttırmaya ikincil olarak bellek oluşumunda rol oynayabileceği, ikisinin bağımsız araçlarla düzenlendiği görülmektedir.
- cAMP aktivitesi : Adenosin trifosfatın (ATP) bir türevidir ve cAMP’ye bağlı yolağı taşıyan birçok farklı organizmada hücre içi sinyali dönüştürmek için kullanılır.
Tersine, agmatin NMDA reseptörlerinin zıtlığı [252] [253] ve nitrik oksit metabolizması üzerindeki olumsuz düzenlemeyi [254] gibi bazı hafıza yitirmesine sebeb olan mekanizmalara sahiptir, çünkü her ikisi de pozitif olarak bellek oluşumuna aracılık etmektedir. NOS bastırması gerçekten 40 mg / kg’lık enjeksiyonlarla kaydedilmiştir (L-sitrulin’de azalma, bu da NOS yoluyla daha az arjinin-sitrülin dönüşümünün göstergesidir). [255] İlginç bir şekilde, öğrenme süreci boyunca dentate gyrus ve prefrontal kortekste sitrulin yüksekliği saptanabilir. [243]
- NOS : Nitröz olarak bilinen nitröz oksit, N-O formülüne sahip bir nitrojen oksit olan kimyasal bir bileşiktir. Oda sıcaklığında, hafif metalik kokusu ve tadı olan renksiz, yanıcı olmayan bir gazdır.
- Dentate gyrus : Hipokampus olarak bilinen bir beyin bölgesinin parçasıdır.
Agmatin glutamat (NMDA reseptör zıtı ) ile normal eksilmeyen koşullar altında birlikte serbest bırakılsa da, muhtemelen bir endişe değildir; Öğrenme görevleri sıçan beyinde [241] bazal sinaptik agmatini 0.25μM’den 0.75μM’ye arttırırken, NDMA reseptörünü bastırmak için IC50 100-300μM aralığındadır. [105] [104] Bununla birlikte, yüksek supplement seviyelerin hipokampusta NMDA reseptörlerini bastırabiliceği akla yatkındır.
- IC50 : Bir maddenin belirli bir biyolojik veya biyokimyasal işlevi bastırma gücünün bir ölçüsüdür.
Unutkanlık olarak şüpheli olabilecek bazı mekanizmalar vardır, çünkü NDMA ve NOS (agmatin bastırır) bellek oluşumunu pozitif olarak modüle edebilir. Bu bilginin pratik önemi bilinmemektedir.
Uzamsal öğrenmeyi değerlendirmek için su labirenti kullanan çalışmalar için, hipokampusa doğrudan mikroenjeksiyonlar ile bellek oluşumunu arttıramadı [256] ve bu başarısızlık, karıniçi 10-50 mg / kg enjeksiyonlarında da görülmektedir [258] [259] [260] Agmatin, mekânsal öğrenmeyi değiştirme gibi gözükmemektedir ve keşif öğrenmeyi değerlendiren bir çalışma da benzer bir başarısızlık bulmuştur. [259]
Bağlamsal korku durumu ve öğrenmenin agmatin enjeksiyonları (20-40 mg / kg damariçi olarak) [257] [258] ile bastırıldığı, ancak engelleyici sakınma görevlerinin [244] [244] ve davranışsal öğrenmenin geliştiği görülmektedir. [259] Yerinden gitmiş nesne tanıma (ancak yeni nesne tanıma değil) standart dozaj aralığında (10 mcg 3-4. bel omurları arasındaki aralıktan infüzyon [260] veya 40 mg / kg damariçi [260] de agmatin infüzyonlarıyla geliştirilmiş gibi gözükmektedir.
Bu arada, agmatin’in hafıza oluşumundan fayda sağlayan görevler beyin bölgelerinin normalde öğrenme süreci boyunca (takvime bağlı olmaksızın) agmatin atımlarını gördükleri görevlerdir. Buna, perirhinal korteks ve hipokampus (yerinden edilmiş nesne tanıma) [247] ve prefrontal korteks (davranışsal öğrenme) [245] [246] dahildir; oysa locus coeraleus agmatin takviyesine tepki verdiği bilinmekte ve önleyici kaçınma görevleriyle ilişkilendirilmektedir [ 244]
Agmatin ile elde edilen faydalar görev ve gecikmeye bağlı olarak ortaya çıkarlar ve basit görevlerden ziyade daha karmaşık olanlarla ilişkili olduğu hipotezi ileri sürülür. [261]
Agmatin, agmatin’e cevap veren veya aktifleştirildiğinde yüksek konsantrasyonlarda agmantinin sınıra salınmasıyla bilinen beyin bölgelerindeki bilinci arttırdığı görülmektedir. Bu agmatin, önleyici kaçınma görevlerine, yerinden edilmiş nesne tanımaya ve davranışsal öğrenmeye fayda sağlar; Mekansal öğrenmeyi etkilediği görülmemektedir ve bağlamsal korku durumu (olumsuz uyaranlardan kaçınmayı öğrenme veya korkma) karşı olumsuz olabilir
Muhtemelen bir çan eğrisi etkisi vardır ve daha yüksek dozlar daha iyi değildir ve hala çalışma belleğinin agmatin takviyesi ile arttırıldığına dair bir kanıt bulunmamaktadır.
3.16. Epilepsi ve Konvülsiyon
Nitrik oksit sinyalizasyonunun, nöbetlerin pozitif bir arabulucusu olduğu bilinmektedir [262], burada L-arginin, NOS bastırması ile zayıflatılacak bir şekilde, nöbet duyarlılığını artırır (diğer şeyler kendiliğinden başlayınca). [263] Agmatinin α2A reseptörü vasıtasıyla nöbet frekansını ve büyüklüğünü azaltmak için nitrik oksit üretimini azalttığı (iNOS’u aşağıya düzenleyerek ) işaret ettiği düşünülmektedir [264]
- iNOS : İltihaplanma koşullarında ortaya çıkar ve büyük miktarlarda Nitrik oksit üretir
Bir nöbet meydana geldiğinde, nitrik oksit sinyali artar ve aşırı Nitrik oksit sinyali, nöbetin bir hastalıktan kalan doku bozukluğu arttırır. Agmatin’in, adrenerjik reseptörü, α2A reseptörü üzerine etkimeyle sonuçlanan NO sinyali miktarını azaltarak nöbetlerin koruyucu olduğu düşünülmektedir.
Agmatin’in kendisi (nöbet uyarımından 45 dakika önce 100 mg / kg enjeksiyon), fenobarbitolü (Epilepsi için bir çeşit ilaç) ( 22.54’ten 16.82 mg / kg’a düşürüldü) ve valproat’ı (Epilepsi için bir çeşit ilaç) (256.1 ila 210.6 mg / kg) nöbet bastırmasını artırabiliyor; Elektrik şoku (MES) uyarımlı nöbetler [265] ve diğer test edilen antiepileptikler (karbamazepin, lamotrijin, fenitoin, okskarbazepin ve topiramat) agmatin’den etkilenmedi. [265]
Daha düşük dozlarda agmatin (30 mg / kg oral sindirimi ) ile MES uyarılan nöbetleri 15 dakika içinde azaltmada etkili olduğu belirtilirken, başka yerlerde karşılaştırılabilir dozlarda enjeksiyonlar (80-160 mg / kg, ancak daha düşük değil) MES’e karşı anti-konvülsif idi [266] Ve altı saat (dört saatte en etkinlik [264]) ve 60-120 mg / kg’da 30 mg / kg’dan anlamlı olarak daha etkili değildi. [264]
Pentilmetetrazol ( Epilepsi için kullanılan ilaç) (PTZ) uyarılan nöbetler öncesinde daha düşük agmatin (5-40 mg / kg, nöbetten 30-45 dakika önce 10-20 mg / kg en yüksek etkinlik) antikonvülsif etkilere [263] sahip olduğu zayıflatılmış şekilde gösterilmiştir [263] Yohimbine ve nitrik oksit uyarımı ile, ancak NOS engelleyicisi L-NAME ile güçlendirildi. [263]
Agmatin, kemirgenlerde çoklu uyarıları (PTZ ve MES) takiben nöbetlerin bastırılmasında aktif gibi görünmektedir ve bu kısa süreli oral dozlamanın 15-360 dakika içinde sıçanlarda meydana geldiği teyit edilmiştir; Tahmini beşeri eşdeğer 5 mg / kg vücut ağırlığıdır
3.17. Kalsiyum Sinyali
Agmatin’in kalsiyum sinyaliyle birkaç etkileşimi vardır. Birincisi, NMDA reseptörü aktivasyonu, daha sonra nNOS’u [267] [268] aktive edebilen ve NDMA karşıtları olan [105] agmatin, hücre içi kalsiyumu arttırma eğilimi gösterir. [105] Agmatin, kalsiyumdaki artışı sınırlayabilir (agmatin nNOS üzerinde bu şekilde davranabilir). Ayrıca, agmatin’in hippokampal nöronlarda doğrudan 0.79-1.57μM IC5o değeri ile tersinir bir şekilde kalsiyum kanallarını bloke ettiği ve 100 nM konsantrasyonda 21 ±% 4 bastırma gösterdiği bildirilmiştir [225]; ancak başka yerlerde Diltiazem olarak bilinen kalsiyum kanal blokeri yerini alacaktır. [269]
- IC5o : Bir maddenin belirli bir biyolojik veya biyokimyasal işlevi bastırma gücünün bir ölçüsüdür.
Agmatin, 500μM’ye kadar konsantrasyonlarda sodyum veya potasyum kanalları üzerinde herhangi bir etkiye sahip olmamıştır. [225] Bununla birlikte, nitrik oksitin, NMDA aktivasyonunun akış aşağısında olan [270] [271] kalsiyumla aktive olan potasyum kanallarının aktivitesini arttırdığı kaydedilmiştir [272], bu, agmatinin potasyum kanallarında bastırıcı bir etkisini varsaymaktadır (çünkü NMDA karşıtları ), antidepresan etkilere en azından kısmen katkıda bulunduğu düşünülmektedir. [215]
Genel olarak, agmatinin kalsiyum sinyali ile (hem NMDA sinyalini önleyerek, hem de fizyolojik konsantrasyonlarda akışı doğrudan bastırarak) karşıt olduğu görülmektedir ve dolaylı olarak potasyum kanalı sinyallemesini (aynı zamanda NMDA zıtlaşması yoluyla) bastırabilir.
3.18. Diğer Mekanizmalar
Diyabetik toksin streptozotosin tarafından uyarılan hafıza defisitleri olan farelerde 30 gün süreyle düşük doz agmatin (5-10 mg / kg enjeksiyon), hem kan glukozunu düşürebilir hem de hafızayı iyileştirebilir [273] ancak hafıza geliştirme etkisi I2 ( Imidazolin) reseptöründen bağımsızdır , [273] (iki bağımsız mekanizma olduğunu düşündüren) glukoz azaltımı için gereklidir. [274]
Agmatin ayrıca beta-amiloid pigmentasyonu, MPTP toksini [276] skopolamin (derin uykuya neden olan bir ilaç) [277] [278] ve iltihaplanma ile uyarılan hafıza bozukluğuna karşı koruyucu etkiler göstermiştir. [275]
- Beta-amiloid :Alzheimer hastalarının beyinlerinde bulunan amiloid plakların ana bileşeni olarak Alzheimer hastalığında çok önemli rol oynayan 36-43 amino asitten oluşan peptidleri ifade eder.
- MPTP toksini : Beyindeki substantia nigrada dopaminerjik nöronları yok ederek Parkinson hastalığının kalıcı semptomlarına neden olan nörotoksin MPP + ‘nın bir ön ilacıdır. Çeşitli hayvan çalışmalarında hastalık modellerini incelemek için kullanılmıştır.
Agmatin, beynin unutkanlığı oluşturan araştırma toksinlerinden ve hafıza oluşumuna karşı olumsuz olabilecek koşullardan (iltihaplanma ve kan şekeri yükselmesinden) korumayı başarıyor görünmektedir.
- PPI : Ana hedefi mide asidi üretiminin belirgin ve uzun süreli bir azaltımı olan bir ilaç grubudur.
İki çalışma agmatinin prepulse bastırması (PPI) bozmak için bir kabiliyet sergilediğini, bunun bir ‘prepulse’, genellikle bir nöronal aksiyon potansiyeli, istenen aksiyon potansiyeli veya nabızdan önce zayıf olarak oluştuğu ve duyarsızlaştırmanın sinyali zayıflattığı bir fenomen olduğunu belirtmiştir [281] ]).
PPI yüksek olduğunda aktif aksiyon potansiyeline sahiptir ve PPI düşük aktif olduğunda biraz nemlendirilirler. Kesilmiş prepulse bastırmasının şizofreni ile ilişkili olduğu düşünülmektedir [282] [283] ve anksiyete ve Travma Sonrası Stres Bozukluğu gibi diğer nörolojik rahatsızlıklar şizofreni hastalarının kanında agmatin konsantrasyonları da artmaktadır [68]
Araştırma hayvanlarına agmatin enjeksiyonu, agmatin’in PPI’yi sesle [284] ve ilaç fensiklidinle hafifletebildiğini belirtmiştir [285] Bu konuda apomorfinin (d2 reseptörlerini uyararak kusmaya çalışan bir ilaç) katkısı vardır [284] ve sıçanlara agmatin verilmesi, apomorfinden uyarılan zirve noktasını ve amfteamin / ketaminin uyardığı aşırı hareket kabiliyeti hafifletebilir [286]
Agmatin ve ön uyarıcı bastırmasının etkileşimleri vardır, bunlar nörolojik bir fenomen olup, daha küçük bir ‘ön uyarıcılar’ oluşur ve kısa süreli duyarsızlaşma nedeniyle sonraki ‘ön uyarımın’ büyüklüğünü bastırır.
4 Uzun Yaşam ve Ömrü Uzatma
4.1. Nörolojik Yaşlanma
Yaşlanma sürecinde ön kortekste toplam NOS aktivitesi (enzim sayımı değil) arttığı için nitrenerjik (nitrik oksit ile ilgili) düzensizlik var gibi gözükmektedir [287], ön korteks ve hipokampusta (CA1 hücreleri) agmatin azalmaktadır ve [287] ) [288] yanı sıra poliaminlerin artışıda. [289] NOS’da bulunan artışın ve agmatinin azalmasının yaşla ilişkili davranış bozukluklarıyla ilişkili olduğu düşünülmektedir. [290] [292]
- CA1 :Öncelikle beyin, omurilikte sinir hücreleri üzerinde bulunurlar, fakat aynı zamanda bazı periferik organlarda ve dokularda bulunurlar.
- Poliamin :DNA, RNA ve proteinler gibi negatif yüklü moleküller ile etkileşime giren polikatyonlardır.
- eNOS :İnsanlarda kromozom 7’nin 7q35-7q36 bölgesinde yer alan NOS3 geni tarafından kodlanan bir enzimdir.
- nNOS : Merkezi sinir sistemindeki sinaptik plastisiteyi (CNS), kan basıncının merkezi düzenlenmesini , düz kas gevşemesini ve periferik nitrerjik sinirler yoluyla damar genişlemesini içerir.
Yaşlı sıçanlarda 4-6 hafta boyunca günlük Agmatin enjeksiyonları (40mg / kg), eNOS veya nNOS protein içeriğini etkilemeksizin (yaşlanma sürecinden önemli ölçüde etkilenmeyecek şekilde) dentat girus ve ön kortekste artmış NOS aktivitesini normale döndürmektedir [293 ] Agmatin olarak yukarıda bahsedilen teori ile iyi çalışan bu dozun yaşla ilişkili davranış bozukluklarını düzelttiği de bilinmektedir. [259]
Agmatin, yaşla ilişkili davranışsal eksiklikleri normalleştirmede yararlı olabilir.
5 Kalp ve Dolaşım Sağlığı İle Etkileşimleri
Agmatin, çoğunlukla nitrik oksit ile olan etkileşimlerden dolayı kardiyovasküler sağlığı her iki yönde de düzenlediği görülmektedir. Takip eden bölümlerde, pozitif düzenleme, nitrik oksit aktivitesini arttırmak (ve damar genişlemesi) için kullanılırken, negatif düzenleme, nitrik oksit aktivitesi veya kan damarlarının daralması üzerindeki bastırma etkilerini ifade eder
5.1. Olumlu Düzenleyici Mekanizmalar
Agmatin, damar genişletici maddesidir ve 10uM’de endotel hücrelerinde nitrik oksit üretimini artırabilir [294] ve hücrelerdeki cGMP konsantrasyonlarını artırabilir (nitrik oksitin reseptörü üzerinde normal bir etkisi vardır). [295] Nitrik oksit üretiminin (L-Arginin ve D-Arginin’e benzer şekilde) doğrudan uyarımı, α2A reseptörüne ikincil olarak bulunmuştur ve rauwolscine tarafından reseptör düzeyinde bloke edilmiştir [294]. Arginin, bu reseptörü 1 mM konsantrasyonda aktive ederken, agmatin konsantrasyonu, 100 kat daha düşük seviyede olmalıdır. [294]
- cGMP : Döngüsel AMP’ye benzeyen ikinci bir haberci gibi davranır. En muhtemel etki mekanizması, hücresel-geçirgen olmayan peptid hormonlarının dış hücre yüzeyine bağlanmasına yanıt olarak hücre içi protein kinazların aktivasyonudur.
Agmatin esas olarak α2A reseptörüne etki ederek nitrik oksit sentezini başlatır. Bu, L-arginine (ve uzatma olarak L-sitrulin) benzer bir mekanizma olmasına karşın, bu reseptörü aktive ederken agmatin 100 kat daha kuvvetli görünmektedir.
Nitrik oksitin genel üretimi, NOS enzimlerinin önleyicileri nitrik oksit üretimini ortadan kaldırdığı için G proteini sinyalleşmesine (α2A reseptörüne bağlı Gi / o) ve Nitrik oksit enzimine bağımlıdır [296] Kalsiyum kanallarını modüle eden [297], kalsiyum kanal aktivasyonu [91] [294] ve riyanodin reseptörleri (RyR) de rol almaktadır.
Agmatin ve RyR’lerin (nitrik oksit tarafından aracılık edilen) etkileşimi nitrik oksitin siklik ADP-riboz (cADPr) aktivitesini arttırması nedeniyle olabilir; [299] cADPr, RyR’nin pozitif bir düzenleyicisidir [300] [301] Ve agmatin seviyelerini etkilemez veya cADPr’in eylemlerini ortadan kaldıran bağlanması [302], nitrik oksit oluşumunu engeller. [302] Buradan, kalsiyumun yükselmesi, kalmodulin olarak bilinen proteinin harekete geçirilmesi nedeniyle eNOS enzimlerinin aktivitesini artırabilir [303] [304].
- G proteini :Hücrelerde önemli sinyal transdüksiyon molekülleridir.
- RyR : Kaslar ve nöronlar gibi uyarılabilir hayvan dokularının çeşitli formlarında bir hücre içi kalsiyum kanalı sınıfı oluştururlar.
- cADPr : Kalsiyum sinyallemesi için bir hücresel habercidir.
Α2A reseptörünü aktive ederek nitrik oksitin arttırılması, α2A reseptörüne bağlanmış G-proteininin cADPr olarak bilinen ve ardından riyanodin reseptörünün aktivitesini arttıran bir moleküle etki etmesini gerektirir. Riyanodin reseptörü kalsiyumu serbest bırakır ve bu kalsiyum daha sonra kalp modülünü harekete geçirerek endotel nitrik oksit sentazini (eNOS) ve ardından nitrik oksit üretimini harekete geçirir.
Yukarıdaki problem, riyanodin reseptörlerinin (RyR’ler) nitrik oksit oluşumuna hem bağımlı hem de uyardığıdır, bu da NOS enzimlerinin hem yukarı hem de aşağı akışında olduğunu göstermektedir [306] NOS enzimlerini bastırma , aslında agmatin’in RyR’ler üzerinde etkili olmasını engeller. [302] İlginç olarak, nitrik oksit üzerindeki agmatinin etkileri, NOS bastırmasından bağımsız olan imidazolin reseptörlerini, [91] fosfolipaz C (PLC), [294] ve PI3K [199] engelleyerek bozulmuş olduğu da belirtilmiştir . [295]
PI3K ve PLC’ye yönelik imidazolin [307] ve α2A reseptörlerinden [308] sinyal oluştuğu bilinmekte ve, Akt yoluyla PI3K’den eNOS aktive eden bir sinyal yolağı var [309] [310] ve agmatinin bu yolla sinyal verdiğini gösterdi. [311]
- PLC : Fosfat grubundan hemen önce fosfolipidleri ayıran hücreyle ilişkili enzimlerin bir sınıfıdır.
- PI3K / Akt : Kas protein sentezini tetiklemek üzere aktive olan proteinler
Riyanodin reseptörünün aktivasyonu aslında nitrik oksit gerektirir (hem NOS enzimlerinin hem yukarı hem de aşağı tarafındadır) ve bu, hem α2A hem de imidazolin reseptörleri vasıtasıyla sinyal göndererek PI3K / Akt / eNOS yolağının aktivasyonuna neden olan rasyonal olabilir ve bu da üretim miktarını artırabilir .
PI3K / Akt / eNOS yolağının aktivasyonunun nitrik oksit sentezinde kısa bir artışa neden olduğu, daha sonra artmış nitrik oksit daha sonra RyR / kalmodulin yolağını aktive ederek daha uzun süreli bir destek sağladığı akla yatkındır.
- Kalmodulin : Tüm ökaryotik hücrelerde eksprese edilen çok fonksiyonlu bir ara kalsiyum bağlayıcı mesajcı proteindir.
5.2. Olumsuz Düzenleyici Mekanizmalar
Ayrıca agmatinin bazı pro-kontraktil özellikleri vardır. Yüksek konsantrasyonda agmatin (1 mM), klonidin prokontraktil özelliklerini (0.9 μM ila 2.6 μM) baskı altına alırken noradrenalinin arterlere temas yeteneğini hafifçe artırabilir (2.2 μM’den 1.5 μM’ye EC50 değer değişimi) ve Metoksamin (1.6μM ila 2.8μM). [102]
- EC50 :Yarı maksimum tepki veren bir ilacın konsantrasyonudur
Agmatin, yüksek konsantrasyonlarda noradrenalinin kontraktil özelliklerini artırabilir
220 um (iNOS), 660μM (nNOS) ve 7500μM (eNOS) Ki değerlerine sahip NOS’un tüm izoformlarında zayıf rekabetçi bastırma olduğu görülmektedir. Diğer çalışmalar, nNOS ve eNOS’un bastırmasını bulamamış olmasına rağmen nNOS’u 160uM [43] IC50 ve 260μM [312] ile iNOS ile bastırmıştır. [312] Diğer çalışmalar çoğunlukla bastırma için gerekli olan yüksek konsantrasyona bağlı olarak muhtemelen NOS enzimleri (özellikle de eNOS, hiç de bastırılmamış gibi görünmektedir) [46] [45] [44] üzerindeki engelleyici etkileri kendiliğinden bulamadılar .
Agmatin, NOS enzimlerinin aktivitesini bastırabilir , ancak bu oldukça yüksek konsantrasyonlarda gerçekleşir; INOS ve nNOS’un bastırması takviye olmadan mümkün değildir (fakat takviye ile uygulanabilir), eNOS’un bastırması önemsiz gibi görünmektedir (maddeye göre konsantrasyon çok yüksektir)
Zayıf rekabetçi bastırmasına rağmen, agmatin’in 29 μM Ki ile geri dönüşümsüz nitrik oksit sentezi (NOS) enzim inaktivatörü olduğu bilinmektedir. [116]
Mekanizma, NOS’un NADPH oksidaz alt kümesinin (bu çalışma, nNOS kullanılmıştır) etkinliğinde 3 kat artışa ve bu da enzimin H2O2 ve oksidatif inaktivasyonuna neden olmuştur. [116] Bu, bir elektronu NADPH oksidaz altbiriminden NOS enziminin heme grubuna aktaran kalmodulin’e, kalmodulinin de inaktivasyon yoluyla NOS aktivitesini azaltabileceğine [116] ve bir saatlik aktivitenin 30 ± 1.2’ye düşürülmesine bağlıydı , NADPH’yi atlamak ilk 20 dakika için bir etkisinin olmamasına karşın 20-60 dakika arasında inaktivasyonu belirgin olarak bastırdı. [116]
- NADPH : Hücre dışı boşluğa bakan hücreye bağlı bir enzim kompleksidir.
- H2O2 : Hidrojen peroksit, H ₂O ₂ formülüne sahip kimyasal bir bileşiktir. Saf haliyle, soluk mavi, berrak bir sıvıdır, sudan biraz daha viskozdur. Hidrojen peroksit en basit peroksittir
Negatif düzenlemenin bu genel profili (zayıf rekabetçi engelleyici , ancak bir oksidatif inaktivatör), aminoguanidin [313] ve guanabenz gibi diğer NOS engelleyicilerine benzerdir. [315] Bunun, agmatin’in kısa plazma yarılanma ömrü nedeniyle biyolojik olarak ne kadar önemli olduğu bilinmemekle birlikte, enzim bastırmasının aksine inaktivasyon fizyolojik açıdan önemli bir konsantrasyonda gerçekleşmektedir.
Agmatin, NOS enzimlerini inaktive edebilir ve bu, çok daha makul bir dozajda (eNOS’u aktive eden üç kat) meydana gelir. Bu inaktivasyonun, canlı bir sistemde nitrik oksit üretimini nasıl etkilediğinden tam olarak emin değiliz.
5.3. Kalp Dokusu
İzole ventriküler miyositlerde, agmatin (0.1-10 mM), hücrelere kalsiyum alımını bastırdığı ve L-tipi kalsiyum kanalının tepe geniş konsantrasyona bağlı olarak azalttığı kaydedildi. [317]
Yüksek konsantrasyonlarda izole hücrelerde kalsiyum bloke etme etkisi vardır. Bu bilginin pratik önemi henüz bilinmiyor.
5.4. Kan Akışı ve Pıhtılaşma
Damar genişlemesi, böbrek hücrelerinde (glomerüler filtrasyon hızında bir artışa neden olur) kaydedilmiştir [318] [306] ve kalp hücreleri (aortik halkalar) [319] [320] nitrik oksit bağlı gibi görünmektedir. (NOS engelleyicileri tarafından engellenmiş ve endotele bağımlı). [296]
- Glomerüler filtrasyon : Böbreklerin ne kadar iyi çalıştığını belirleyen bir testtir.
Agmatin infüzyonları sıçan arteriyel kuyruk damarındaki damar tonusu değiştirmediler. [102]
Canlılarda bazı nitel oksit’e bağlı bazı rahatlatıcı özellikler gösterir
300μg / kg agmatin verilen sıçanlarda kanama süresini değerlendiren bir çalışma kan incelticileri tarafından arttırıldığını ve kanamayı takiben kan basıncında bir artış olduğunu ve bunun da hayatta kalmayı artırdığını ve bu etkinin yohimbin ve arginin tarafından ortadan kaldırıldığını belirtti (α2A’ya bağlı olduğunu ve Nitrik oksitin bir indirgenmesi). [321]
Kan akışında tek taraflı bir artış değil, kan akışında genel bir düzenleyici rolünün olduğunu düşündüren kan basıncındaki artış ile ilişkili kanamayı azalttığı görülüyor
5.5. Kan Basıncı
Agminatin, hem α2A reseptörlerinde hem de imidazolin reseptörlerinde klonidinin yerini aldığı ve klonidin’in imidazolin reseptörü vasıtasıyla bir antihipertansif (kan basıncını düşüren) ilaç olarak işlev gördüğü bilinmesinden dolayı, klonidin yer değiştirme maddesi olarak bilinir. [322] [323] [324] Tuhaftır ki, imidazolin reseptörü agmatin’inden klonidin yer değiştirmesine rağmen, onun hareketlerine müdahale etmez. [73]
İmidazolin reseptörlerine müdahale kan basıncını düşürdüğü bilinmektedir
Uyuşturulan sıçanlarda, agmatin enjeksiyonları kan basıncını düşürdüğü görülmektedir [73] [325] [326]
6 Glukoz Metabolizması ile Etkileşimleri
6.1. Kan Şekeri
Adrenal bezde yerelleşmiş olan imidazolin reseptörlerinin aktivasyonunun, streptozotosin (bir tür antibiyotik) kaynaklı diyabetik sıçanlarda kan glukozunu azalttığı bilinmektedir ve agmatinin bu reseptörleri aktive ettiği bulunmuştur. [92] [274] Kan glukozundaki azalmanın β-endorfinin artışı ile ilişkili olduğu düşünülmektedir [274] [92] ve β-endorfinin egzersiz yapıp yapmamasından bağımsız olarak iskelet kasına [327] [328] doku glukoz alımını arttırdığı bilinmektedir [329] muhtemelen GLUT4 mRNA içeriğindeki bir artışa bağlı olarak. [274]
- β-endorfinin : Merkezi sinir sistemi ve periferik sinir sistemi içinde belirli nöronlarda üretilen dahili bir opioid nöropeptid ve peptit hormonudur.
Β-endorfinin başka yerlerde hepatik glikoz üretimini bastırdığı [330] pankreasdan insülin salgılanmasını oluşturduğu bildirilmiştir [331] ancak agmatin takviyesinin bu parametreleri nasıl etkilediğinden emin değildir.
Agmatin, β-endorfini, kandaki glikozu iskelet kası dokusuna atabilecek bir opioidi serbest bırakmak için adrenal bezleri (imidazolin reseptörleri vasıtasıyla) hareket ettirebilir. Bu nedenle, agmatin, adrenal bez bağımlı yollarla kan şekerini azaltabilir
7 İskelet Kası ve Performansı
7.1. Mekanizmalar
Adrenal bezler üzerine aktive olan imidazolin reseptörlerine ikincil olan agmatin, β-endorfini plazma içine salabilir. [274]
Β-endorfinin (agmatin bağlı) diyabetik sıçanlarda iskelet kası glukoz alımını arttırdığı bilinmektedir [274] [92] kasın dinlenip durmadığından bağımsız olarak [329] muhtemelen GLUT4 mRNA yukarı düzenlenmesi yoluyla [274] β-endorfin (Tek başına, bu çalışmada agmatin bağlı değildir), yağ dokusunda glukoz alımını değiştirmediği görülmüştür; [332] bu muhtemel bir besleyici bölümleme etkisini önerir, ancak onaylamak için daha fazla araştırılması gerekir.
Agmatin, diyabetik hayvanlarda kan glukozunu keskin bir şekilde azaltabilir ve bunun β-endorfinin artmasına bağlı olarak yağdan ziyade kana glikozun seçici bir şekilde atılmasından kaynaklandığı akla yatkındır. Bunun oral eklenmeyi takiben gerçek olup olmadığını değerlendirmek için daha fazla çalışma gerekmektedir.
8 Hormonlarla Etkileşimi
8.1. Lüteinleştirici Hormon
Agmatin’in hipotalamusa enjeksiyonu, aktive edici imidazolin reseptörlerine ikincil olarak düşünüldüğü düşünülen dozaja bağımlı olarak lüteinizan hormon salgısına neden olur. [333]
9 Vücut Organları İle Etkileşimi
9.1. Gözler
Deney Ortamında agmatin retinal ganglion hücrelerini doku ölümünden korur [334] ve göz basıncın azalmasıyla ilişkili görünen topikal olarak uygulanmış agmatin (% 55.44 hücre ölümünü% 18.65’e düşüren) ile belirtilmiştir [335] ] Bu koruyucu etki aynı zamanda kansızlık göz yanmasına da neden olur. [336]
Topikal olarak uygulanan agmatin, gözler için koruyucu olduğu görülmektedir; Oral eklemenin sonuçları henüz bilinmiyor
9.2. Mide
Agmatin genellikle sıçanlarda (dalakların ve bağırsakların önünde) agmatinin en yüksek beyin dışı organ konsantrasyonlarından biri olan yaklaşık 71ng / g yaş ağırlıklı bir konsantrasyonda mide dokusunda ifade edilir. [27] Karnın mukus zarlarında depolanır ve burada güçlü alkalinite zararlı parietal hücrelere mide asidini muhtemelen tamponlar. [23]
Agmatin, midenin parietal hücrelerini mide asidinden koruduğu alkalinite dolayısıyla mide koruyucu olarak görünür.
100 mg / kg’lık agmatin (enjeksiyon) gastrik kansızlığa karşı koruyucu etkiler göstermiştir, [337] ancak başka yerlerde, alkol ile uyarılan ülserasyon [338] ve imidazolin üzerine etki ederek strese bağlı ülserasyon [339] [340] üzerinde hasar görmüştür 20-25mg / kg doz aralığında reseptörler; Farkın sebebinin yaranın dozajı veya bağlamından kaynaklanıp kaynaklanmadığı açık değildir.
Α2A reseptörleri önemli rol oynamayan imidazolin reseptörleri ile aktive edildiğinde gastrik kasılmaları uyardığı görülmektedir. [341]
Agmatin hem mideyi hasardan (kansızlığa karşı) korumakta, hem de kimyasal ve stresle uyarılan hasarla oluşan hasarı arttırmaktadır.
9.3. Bağırsaklar
Agmatin, kolonik bakteriler (ayrıca mide bakterileri [342] tarafından üretildiğinden) bağırsaklarla ilgilidir ve agmatin’in oral yolla verilmesinden sonra bağırsaklarda birikebilir. [70]
9.4. Böbrekler
Agmatin, muhtemelen I2 imidazolin reseptörleri vasıtasıyla böbrek dokularında glomerüler filtrasyon hızını artırabilen böbrekte üretilir [318] ve başka yerlerde NOS enzimlerine bağımlı olduğu bulunmuştur [296] 2-adrenerjik reseptörlere ihtiyaç duyulmamaktadır [318] [296] fakat riyanodin reseptörleri olarak bilinen bir sınıf reseptörün aktivasyonu (kalsiyum sinyalini aktive eder) agmatin’in etkilerini açıklayabilir. [302] Mekanizma ne olursa olsun, sinir hücrelerinin gerekli olmadığı görülmektedir. [318]
- Glomerüler filtrasyon : Böbreklerin ne kadar iyi çalıştığını belirleyen bir testtir.
Na + / K + ATPaz’ın böbrek hücrelerde arttığı da kaydedilmiştir. [343]
Ön kanıtlar, muhtemelen bir böbrek -koruyucu etkisi olan glomerüler filtrasyon hızlarında bir artış olduğunu düşündürmektedir. Bu, riyodin reseptörleri üzerinde etkili olan nispeten yeni bir mekanizma ile ilgili olabilir.
9.5. Erkek Cinsel Organı
Agmatin’in potasyum kanallarını 10-1,000 μM’de bloke etmeyle ilişkili olduğu düşünülen elektriğe bağlı sürtünmeleri geliştirebildiği sperm tünelindeki α2A reseptörleri [144] ile presinaptik ve postsinaptik olarak etkileşime girdiği bilinmektedir. [344] [345] Daha sonra, bu artışın sperm tünelindeki prostatik kısmında oluştuğunu, ancak epididimal kısmın oluşmadığını ve 1mM’de maksimum kontrole ulaştığını belirtti (kontrolün 207.1 +/- 14.2%). [345]
10 Besin-Supplement Etkileşimleri
10.1. Arjinin / Sitrülin
L-Arginin ve L-Citrulline plazma arginin konsantrasyonlarını artıran iki amino asittir.
Agmatin’in nitrik oksit sentez enziminin oksidatif inaktivasyonu (bu çalışmada 29 μM Ki ile nNOS ile görülmüştür), argininin nNOS’u engellediği bilinen NADPH oksidaz altbiriminin [116] aktivitesini arttırdığı için [117] [118] Ancak iNOS ve eNOS için etkinliği artırdığı görülmektedir. [346] [117] Bu anlamda, arginin, agmatin’in nNOS’a karşı etkileri ile zıttır (supplement argininin birçok nörolojik etkiyi bastırmasının muhtemel bir nedeni) ancak eNOS’u aynı şekilde etkilememektedir.
- nNOS : Merkezi sinir sistemindeki sinaptik plastisiteyi (CNS), kan basıncının merkezi düzenlenmesini , düz kas gevşemesini ve periferik nitrerjik sinirler yoluyla damar genişlemesini içerir.
- iNOS :İltihaplanma koşullarında ortaya çıkar ve büyük miktarlarda Nitrik oksit üretir
- eNOS : İnsanlarda kromozom 7’nin 7q35-7q36 bölgesinde yer alan NOS3 geni tarafından kodlanan bir enzimdir.
- NADPH : Hücre dışı boşluğa bakan hücreye bağlı bir enzim kompleksidir.
Bu iki maddenin arginin ile eşleştirilmesinin, sistemik nitrik oksit üretimini (eNOS yoluyla, kan basıncı etkilerinin çoğunun altında yatan mekanizma ile) artıracağından veya zıt olup olmayacağından emin değiliz; Her ikisi de makul olup, birincisi eNOS’tan nitrik oksit üretiminin artması ve ikincisi, enzimin daha çabuk inaktive edilmesinden kaynaklanmaktadır.
Arginin (ve uzatılmasıyla sitrulin), opioid (morfin gibi etkileri olan bir bitki) toleransını azaltmak gibi agmatin takviyesinin nörolojik etkilerinin bazılarını bastırır. Kan damarları (ve fiziksel egzersiz için ‘pompa’) açısından agmatin ve arginin arasındaki etkileşim net değildir.
10.2. Alkol
Agmatin hem mide-bağırsak hem de nörolojik düzeyde alkol ile ilişkilidir ve genel olarak agmatin’in alkol yoksunluğunun iyileştirilmesi için iyi olduğu ancak muhtemelen en iyi koalisyon desteğini vermediği söylenebilir.
Alkolün endişeyi azalması arginin dekarboksilaz enziminin bastırmasını ile engellenir ve agmatin ile işe yaradığını ileri sürer. [174] Alkol çekilmesi sırasında görülen kaygının artışı da agmatin ile normalize edilmiştir. [174]
Ek olarak, alkolün acı yitimi (ağrı kesici) etkileri, sıçanlarda agmatin enjeksiyonu ile imidazolin reseptör sinyalizasyonuna bağlı olduğu düşünülmektedir [347] ve agmatin’in sıçanlarda (sadece erkeklerde) görülen alkol bağımlı hiperaktiviteyi bloke ettiği görülmüştür. [348] Motivasyon / bağımlılık üzerinde herhangi bir değişiklik olmadığının göstergesi olduğu düşünülen agmatin ve koşunlandırılmış yer tercihi (CPP) arasında herhangi bir etkileşim olduğu görülmemektedir. [349]
- CPP : Nesnelerin veya deneyimlerin motivasyon etkisini ölçmek için kullanılan bir Pavlovian koşullandırma şeklidir.
Olumsuz bir yönü olan agmatin’in mide koruyucu bir madde olduğu (parietal hücrelerin mide asidinden korunmasına yardımcı olduğu [23]) bilinmesine karşın sıçanlarda alkol tüketiminden karşı önleyici olarak artmış ülser oluşumu olduğu bilinmektedir. [338]
Agmatin zamanla şu an alkol yoksunluğu için yararlı gibi görünüyor. Agmatin’in alkol ile birlikte kullanılması, bir çalışmada mide ülseri gelişimi olmadığı için tedbirli olmayabilir, bu nedenle agmatin ve alkol tüketiminin zamanlaması ihtiyatlı olacaktır
10.3. Kafein
Hareket yeteneğini uyarabilen (kafeinli farelerde) kafeinin kısa süreli dozları ile 5-20mg / kg’da agmatin, hareket yeteneğindeki artışı ancak sadece erkek farelerde engelleyebildi. [350]
10.4. Esrar
Esrar, endokannabinoid reseptörleri (CB1 ve CB2) olarak bilinen iki reseptör aracılığıyla sinyal veren prototip kanabinoid ilaçtır; Aşağıdaki bilgiler, tüm CB1 karşıtları (muhtemelen arakidonik asit metabolizmasından anandamide ve oleamide) CB2 agonistleri ile belirsiz etkileşimler (ekinezya) için geçerli olmalıdır.
- CB1 Reseptörleri : Öncelikle beyin, omurilikte sinir hücreleri üzerinde bulunurlar, fakat aynı zamanda bazı periferik organlarda ve dokularda bulunurlar.
- CB2 Reseptörleri : CB2 reseptörü, kanabinoidlerin çevresel reseptörüdür.
CB1 reseptörleri, orta beyindeki [131] [132] bir modelde eksprese edilir; bu, imidazolin reseptörlerinin [133] ve agmatin lokalizasyonunun [28] tarzına çok benzerdir ve en azından kalp dokusunda yararlı etkileri olduğu bulunmuştur. bir diğeri. [134]
Endokannabinoid reseptörleri, imidazolin reseptörlerinin yakınında eksprese edilir ve birbirlerini pozitif yönde etkilediği görülür; Esrar CB1 reseptörlerinde güçlü bir aktivatör iken, agmatin, imidazolin reseptörlerinin güçlü bir etkinleştiricisidir.
Agmatinin, hipotermiyi [136] [137] sinerjik olarak arttırdığı ve ısı ağrısını azaltmada (her iki ağrı kesicisinde tek başına agmatin’in etkisiz olduğu) iki kannabinoidergik ilaçların gücünü % 300-440 artırabileceği bulundu [135] Bu etki α2A reseptörlerinden bağımsızdır [135] ve hem imidazolin karşıtları (blokerler) hem de CB1 reseptör karşıtları tarafından bastırırken, NOS veya NMDA bastırması ile ilişkili olma olasılığı düşüktür [139] [138]. [135]
Her iki reseptörün gerekliliği ve imidazolin aktivasyonunun CB1 reseptör karşıtları SR141716A’nın reseptörüne [140] bağlanmasını değiştirme kabiliyeti nedeniyle, imidazolin reseptörlerinin aktivasyonunun, reseptörün pozitif oynak modifikasyonu yoluyla sinyali CB1 reseptörüyle zenginleştireceği akla yatkındır ( Sinyali değiştirmek için reseptörün yapısının değiştirilmesi, pozitif işaretlenmeye, taban çizgisine göre bir artışa işaret eder).
- NMDA : Sinaptik plastisiteyi ve hafıza fonksiyonunu kontrol etmek için NMDA reseptörü çok önemlidir.
- SR141716A : Beyin kanabinoid reseptörünün güçlü ve seçici bir karşıtıdır.
CB1 reseptörü sinyali ile imidazolin reseptörü sinyali arasında sinerjizm var gibi gözükmektedir. Şu anda nasıl çalıştığından % 100 emin değiliz, fakat her iki reseptör de önemli gibi görünüyor ve imidazolin aktive edildikten sonra (daha sonra sinyalleşmeyi arttıran) CB1 reseptöründe yapısal değişikliklerin meydana gelmesi olasıdır. Sinerjizm sadece şu anda ısı ağrısı için kaydedilirken, agmatin marihuana ile sinerjik bir mekanizma çeşidi (en heyecan verici derecede nöropatik ağrı) üzerinde sinerjik olma potansiyeline sahiptir.
11 Korunma ve Yan Etkileri
11.1. Genel
Çalışmalarda rastlanmamış olmasına rağmen, bir MSDS, agmatinin kısa süreli LD50’si farelerde oral yoldan alımın ardından 300 mg / kg, sıçanlarda 980 mg / kg ve tavşanlarda 3200 mg / kg’dır [351]
- MSDS : Potansiyel tehlikeler hakkında bilgi içeren bir belgedir (sağlık, iltihap, reaktivite ve çevre)
- LD50 : LD “Ölümcül Doz” anlamına gelir. LD50, bir kerede verilen bir materyalin miktarıdır, bu da bir grup test hayvanının ölümünün% 50’sine (yarıya) neden olur. LD50, bir malzemenin kısa süreli zehirlenme potansiyelini (akut toksisite) ölçmenin bir yoludur.
Doz tolere edilebilirliğini değerlendiren, 51 günde yapılan bir çalışmada, doz 1,350 g (10 gün), 2,67 g (10 gün sonra), 3,56 g (ondan sonra 10 gün, ardından 21 günlük bakım) kullanan doz, günde üç kez yemeklerle birlikte günlük dozlara bölünerek değerlendirildi Radikülopati ile ilişkili omurgasında sorun olan olan hastalar, birkaç gün sonra doz 3.56 grama çıkınca, seyrek sindirim sistemi rahatsızlıktan başka hiçbir önemli sağlık etkisini not etmemiştir. [167]
- Radikülopati : Bacağa giden bir sinirin ezilmesi sonucu ağrının ortaya çıkmasıdır.
İnsanlarda sınırlı kanıt, ancak şu an bilinen hiçbir yan etkisi yoktur. Bununla birlikte, güvenlik düzeyini belirlemek için yeterli kanıt yok
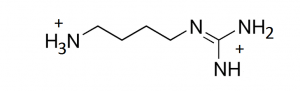
Moleküler Formül: C5H14N4
Moleküler Ağırlık: 130.195 g / mol
(Agmatin için yaygın yazım hataları arasında amatine, agmatin, agatine, agmartine, argmatine )
Bilimsel Destek ve Referans Metni
Agmatin Referanslar
- Biyojenik aminlerin gıdadaki mevcut ve gelişmekte olan yaklaşımlarda kontrolü.
- Agmatin (dekarboksile L-arginin): fizyolojik rolü ve terapötik potansiyel.
- Agmatinin (klonidin-yer değiştiren madde) metabolizması, diamin oksidaz ve imidazolin reseptörlerinin çalışmaları için olası etkileri.
- Odaklı inceleme: fermente gıdalarda agmatin.
- İtalyan kırmızı şaraplarının polifenoller ve biyojenik aminler temelinde doğrulanması.
- Şarapta agmatin ve diğer aminlerin HPLC tayini.
- Alkollü içeceklerde biyojenik aminlerin baskılanmış iletkenlik tespiti ve entegre pulsed amperometrik algılama ile iyon kromatografisi ile belirlenmesi.
- Biranın biyojen amin içeriği; arpa, maltlama ve demleme amin konsantrasyonu üzerine etkisi.
- Kondüktometrik tespiti ile kılcal bölge elektroforezi ile biyojenik aminlerin belirlenmesi.
- Sıradan gıda maddelerinin ve çeşitli fermente gıdaların poliamin içeriği.
- Hazır kahvede biyoaktif aminlerin profili ve seviyeleri.
- Et ve et ürünlerinde biyojenik aminler.
- Kurutulmuş lacón, bir İspanyol geleneksel et ürünü üretimi sırasında biyojenik amin içeriği: Bazı katkı maddelerinin etkisi.
- Şeker içeren ve içermeyen hafif fermente sosislerde biyojen amin ve poliamin içeriğinde değişiklikler.
- Poliaminlerin oluşumu üzerine vakumlu paketlenmiş frankfurterlerin yüksek basınçlı işlenmesinin sonuçları: Soğutulmuş depolamanın etkisi.
- 0 ° C ve 4 ° C’de saklanan barramundi (Lates calcarifer) dilimlerinde biyojenik amin değişmektedir.
- Kontrollü atmosferlerde depolanan ton balığı kırmızı ve beyaz kaslarında serbest amino asitler ve biyojenik aminler.
- Tayland’da farklı pratik endüstriyel yöntemlerin soğutulmuş depolanması altında hamsi (Stolephorus heterolobus) kalite değişiklikleri.
- Yeşil ve kavrulmuş kahvede biyoaktif aminlerin profili ve seviyeleri.
- HPLC ile tahıl ve tahıl bazlı gıda ürünlerinde biyolojik olarak aktif aminlerin izlenmesi.
- 3,5-dinitrobenzoil klorür ile türevlendirildikten sonra fermente gıdalardaki biyojenik aminlerin sıvı kromatografik tayini.
- Agmatin, Nöronal Olmayan Monoamin Taşıyıcıları, Extranöronal Monoamin Taşıyıcı (EMT) ve Organik Katyon Transporter 2 (OCT2) ile Etkin Bir Şekilde Taşınır.
- Gastrik asit üretimi için karbon dioksit kaynağı.
- Imidazolin ligandlarının, saflaştırılmış monoamin oksidaz A’nın aktif bölgesi ile etkileşimleri.
- Bazı merkezi etkili antihipertansiflerin yapı, pKa, lipofilisite, çözünürlük, absorpsiyon ve polar yüzey alanı üzerine teorik çalışması.
- İnsan arjinin dekarboksilazının ifadesi, agmatin için biyosentetik enzim.
- Agmatin sıçan organlarında yaygın ve eşit olmayan bir şekilde dağılmıştır.
- Agmatin, bakteriyel amin, memeli dokularında yaygın olarak dağılmıştır.
- İnsan agmatinazının klonlanması ve karakterizasyonu.
- İnsan agmatinazının klonlanması. Karaciğerde hepatit B virüsü ile başlatılan poliamin sentezi için alternatif bir yol.
- İnsanlarda agmatin homeostazının altında yatan düzenleyici mekanizmalar.
- İnsan agmatinaz, renal hücreli karsinomun temiz hücre tipinde azalır.
- Bernstein HG, ve diğ. Putatif endojen antidepresan agmatinin bir inaktivatörü olan agmatinaz, duygudurum bozuklukları olan kişilerin hipokampal interneuronslarında kuvvetli bir şekilde yukarı doğru düzenlenmiştir.
- Makrofajlarda agmatinin metabolizması: lipopolisakkarid ve inhibitör sitokinler ile modülasyon.
- Ekzojen agmatinin insan lösemi HMC-1 ve HL-60 hücrelerinde proliferasyon, poliamin metabolizması ve hücre döngüsü üzerindeki etkileri.
- İmidazolin reseptörleri ve kan damarlarında agmatin: vasküler düz kas proliferasyonunu inhibe eden yeni bir sistemdir
- Sıçan hipotalamik paraventriküler ve supraoptik nükleusların vazopressin ve oksitosin nöronlarında agmatinin lokalizasyonu.
- Sıçan hipokampüsünde akson terminalleri içeren agmatin, piramidal hücreler üzerinde sinapslar oluşturur.
- Sıçan beyindeki agmatinin bölgesel lokalizasyonu: bir immünositokimyasal çalışma.
- İmidazolin Reseptörleri ve Endojen Ligandları.
- Agmatine karşı bir antikor, sığır adrenal kromaffin hücrelerinde amini lokalize eder.
- Agmatinin gastrointestinal alınması: doku ve organlarda dağılım ve patofizyolojik uygunluk.
- Agmatinin metabolize edilmesi ve sıçan beyninde nitrik oksit içine değil.
- L-arginin analogları ile sıçan serebellum ve makrofajdan saflaştırılmış nitrik oksit sentaz inhibisyonu.
- Sıçan beyindeki nitrik oksit sentaz aktivitesi üzerindeki arginin analoglarının yapı-aktivite ilişkileri.
- İndüklenebilen NO sentazında substrat kaynaklı elektronik, katalitik ve yapısal değişikliklerin analizi.
- Diamin oksidaz, amilorid bağlayıcı proteindir ve amilorid analogları tarafından inhibe edilir.
- İnsan diamin oksidazın yeni bir kristal formu.
- Sıçan hepatosit kültürlerinde agmatinin transport ve metabolizması.
- Sıçan beyindeki bir agmatinaz benzeri proteinin ekspresyonu ve lokalizasyonu.
- Transkarbamilaz ailesine yeni bakış: agirinin fermentatif kullanımı için önemli bir katalizör olan putrescine transkarbamilazın yapısı.
- Agmatin, antimyme ve hücresel poliamin seviyelerinin zayıflatılmasının frameshift indüksiyonu ile çoğalmayı bastırır.
- Sıçan pulmoner arter endotel hücrelerinde ornitin dekarboksilaz aktivitesi ve agmatin ile poliamin transportunun düzenlenmesi.
- Agmatine için yeni bir rol.
- Enterococcus faecalis’in agmatin katabolizması için gen kümesi: rekombinant putrescine transkarbamilaz ve agmatin deiminazın çalışması ve reaksiyonunu katalize eden agmatin deiminazın bir görüntüsü.
- Streptococcus faecalis’in putrescine karbamoiltransferazının yapısı ve özellikleri.
- Streptococcus faecalis’te agmatin bozunması ve sentezlerinin kontrolü enzimleri.
- Bakterilerde arginin biyosentezi ve metabolizması.
- Streptococcus faecalis’in arginin deiminaz yolundaki enzim sentezinin kontrolü
- Escherichia coli’de purin katabolizması ve purin kurtarmasında ksantin dehidrogenazın fonksiyonu.
- KARBAMİL-P ÖZELLİK OXAMAT TRANSCARBAMYLASE’İN BİR STREPTOCOCUSDA PARABANİK ASİT İLE İNDÜKSİYONU.
- Agmatin strese karşı endojen bir faktördür.
- Agmatin, kan-beyin bariyerini geçer.
- Floresan tespiti ile yüksek performanslı sıvı kromatografisi kullanılarak beyin ve plazmada agmatinin belirlenmesi.
- Normal insan gönüllülerin beyin omurilik sıvısında agmatin seviyeleri.
- Metabolik sendromda düşük plazma agmatin seviyeleri.
- Agmatin: Beyinde endojen klonidin yer değiştiren bir madde.
- Şizofreni hastalarında artmış plazma agmatin düzeyleri.
- Depresyonda plazma agmatin ve trombosit imidazolin reseptörleri.
- Sıçan izole edilen mide ve sıçanların in vivo ortamda {(14) C} agmatine maruz bırakılması: mide duvarında birikme ve çeşitli dokularda dağılım . Agmatinin antidepresan etkisi ve olası mekanizması .
- Farede spinal uygulamadan sonra agmatinin farmakodinamik ve farmakokinetik çalışmaları.
- İmidazolin bağlama bölgelerinde endojen bir ligand olan agmatin, klonidin aracılı kan basıncı reaksiyonunu antagonize etmez.
- Poliamin taşıma sistemi memeli hücrelerinde agmatin taşınmasına aracılık eder.
- Agmatin Sıçan Beyninde Mitokondriyal Arginin Dekarboksilaz ile Sentezlenir.
- Endojen ağrı modülasyonu: Endojen NMDA reseptör antagonisti / NOS inhibitörü, agmatin nörofarmakokinetik / dinamik çalışmalar.
- Agmatine: yeni bir nörotransmitter.
- Sıçan beyindeki agmatinaz aktivitesi: agmatinin bozunması için bir metabolik yol.
- Spinal sinaptozomlardan tritiated agmatinin salınımı.
- Agmatinin sıçan beyin sinaptozomlarına alınması: katyon kanallarının muhtemel rolü.
- Omurilik sinir terminallerinden potasyum ve kapsaisin kaynaklı agmatin salınımı.
- Spinal sinir terminallerine agmatin taşınması poliamin analogları tarafından modüle edilir.
- Agmatin (dekarboksile arjinin) sentezlenir ve astrositlerde depolanır.
- Putrescine, zorunlu yüzme testinde ve farelerde kuyruk süspansiyon testinde antidepresan benzeri etkiler üretmektedir.
- Agmatinin fare alfa (2D) -adrenoseptör ile çift etkileşimi: rekabetçi antagonizm ve allosterik aktivasyon.
- Fare zorla yüzme testinde agmatin antidepresan benzeri etkide serotonin reseptör alt tiplerinin tutulumu için kanıt.
- Radyo-ligand bağlanma çalışmaları, agmatinin NMDA reseptöründe bir poliamin sahası için arcain veya ifenprodilden daha seçici bir antagonist olduğunu ortaya koymaktadır.
- NMDA reseptörlerinin poliamin modülasyonu ile ilişkili moleküler özellikler.
- Farelerde beyinde 5-HT1A / 1B reseptörleri, alfa2-adrenoseptörler ve reseptör sonrası adenilat siklaz aktivasyonu, agmatinin antidepresan benzeri etkisinde yer alır .
- İmidazolin ve alfa-2 adrenerjik reseptörlerinde agmatin ve endojen klonidin-yer değiştiren maddenin özelliklerinin karşılaştırılması .
- Endotel hücrelerinde nitrik oksit sentazınagmatin aktivasyonu .
- Agmatin tarafından beta-endorfin salgılanmasının artması, sıçanların adrenal bezindeki imidazolin I (2A) reseptörlerinin aktivasyonu ile indüklenir.
- Alfa-adrenoseptör bağlanma bölgeleri ile sığır akciğer ve beyindeki agmatin ve ham metanolik ekstraktların etkileşimlerinin karşılaştırılması.
- Agmatin, alfa 2 adrenoseptör bağlanma bölgelerini tanır ancak alfa 2 adrenoseptörlerini aktive etmez veya inhibe etmez.
- Alfa (2) -adrenoseptörlerinin, bovin beyin ve akciğer içeren klonidin-yer değiştirici madde metanolik ekstreleri ile aktivasyonu için kanıt yoktur.
- Hipotalamik paraventriküler nükleustaki agmatin sıçanlarda beslenmeyi uyarır: nöropeptit Y’nin katılımı .
- Agmatin farelerde iki depresyon modelinde antidepresan benzeri etkiler üretir.
- İmmediazol (ine) / guanidin ilaçları ile monoamin oksidaz A ve B aktivitelerinin inhibisyonu, sıçan karaciğerinde I2-imidazolin reseptörlerinin etkileşimi ve ayrımı.
- imidazolin ve guanidin türevleri ile MAO aktivitesinin modülasyonu.
- Boyanan adrenal medullada kromaffin hücrelerinde ve mitokondriyal membranlarda adrenerjik olmayan imidazolin bölgelerinin ekspresyonu .












bu kadar detaylı incelemeleri türkiyeye getirdiğiniz için çok teşekkür ederiz
Hocam selamlar,
Yazı gayet verimli;sormak istediğim husus:
Agmetini azaltan madde yohimbin mi?ve nedir bu madde.
Agmetinin vücutta bulunma dozu çok önemli anladığı. Kadarıyla.
Teşekkürler saygılar.