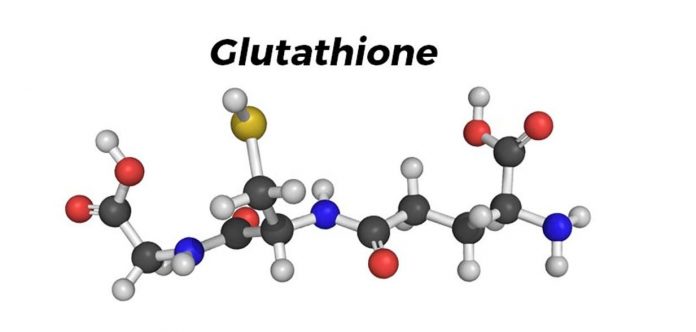
Glutathione (Glutatyon) Nedir ve Ne İşe Yarar ?
Glutathione (Glutatyon), vücudun her hücresinde ve dokusunda kullanılan bir anti-oksidandır. Bir dizi işlem için kritik olmasına rağmen, oral alım sırasında hızlı bozulma nedeniyle diyet supplementi olarak kullanımı sınırlıdır. Metabolitleri L-sistein vücuttaki Glutathione (Glutatyonu) artırabilir, ancak Glutathione (Glutatyon) yoluyla L-sistein tüketimi verimsizdir ve maliyetlidir.
Özet
Tüm Temel Faydalar / Etkiler / Gerçekler ve Bilgiler
Glutathione (Glutatyon) (γ-L-Glutamil-L-sisteinilglisin), bir L-glutamik asit, L-sistein ve Glisin molekülünden oluşan küçük bir amino asit içeren moleküldür (peptiddir). Molekül gıda kaynaklarında ve insan vücudunda bulunur ve burada anti-oksidan olarak işlev görmektedir. ‘Glutathione (Glutatyon) sistemi’, bir hücre içerisinde Glutathione (Glutatyonu) sentezleyen enzimlerin yanı sıra antioksidan etkiler uygulamak için, Glutathione (Glutatyon) kullanan özel enzimleri içermektedir.
Glutathione (Glutatyon) kullanılması, bir hücredeki bu Glutatyon havuzunu desteklediği ve bu nedenle tüm Glutatyon sisteminin etkililiğini koruduğu düşünülmektedir. Glutatyonun hücre biyolojisinde yaygın rolüne rağmen şu anki beslenme supplementinde aşağıdaki farmakokinetik özelliklere bağlı olarak sınırlı bir role sahiptir:
Glutathione (Glutatyonun) bağırsaklardan bir miktar sindirimi olabilir, ancak hücreleri bozulmadan içeri alamazlar. Alınmadan önce L-sistin (iki molekül L-sistein birbirine bağlı) oluşturmak üzere metabolize edilmelidir.
Hücrede L-sistein sağlanması, Glutathione (Glutatyon) sentezini arttırmak için gerekli olanın tamamıdır ve N-Asetilsistein bunu Glutathione (Glutatyona) göre daha düşük maliyetle etkili bir şekilde yapmaktadır.
Aslında, Glutathione (Glutatyon), diyette L-sistein sağlamak için dolaylı ve pahalı bir yoldur. Diyet proteininin kendisi, örneğin Whey Proteini gibi L-sistein açısından zengin kaynaklar da dahil olmak üzere diyette L-sistein alımını artırmak için etkilidir, ancak verimsiz yollar ve N-Asetilsistein Glutathione (Glutatyondan) daha verimli ve ucuzdur.
Oral Glutathione (Glutatyon) supplementi, yukarıdaki nedenlerle hücre içi Glutatyon düzeylerini etkili bir şekilde arttırmazsa da, kan dolaşımına zararsız bir şekilde sindirilebilir. Kanda artmış Glutathione (Glutatyon) düzeylerinin nitrik oksit parçalanmasını yavaşlattığı gösterildiğinden, Glutathione (Glutatyon) supplementi, L-sitrülin veya L-Arginin gibi nitrik oksit artırıcıları, artırmak için yararlı olabilmektedir.
Bilinmesi Gerekenler
N-asetilsistein, Glutathione (Glutatyon) üretmek üzere L-sistein ön ilacıdır.
Glutathione (Glutatyon) Tarihi
1888’de, Rey-Pailhade, maya hücrelerinin, “sülfat” adını verdiği bir madde içerdiğini keşfetti; bu, kendiliğinden sülfür vermek için element sülfür ile kendiliğinden reaksiyona giriyordu. Onun sonraki çalışmaları, hayvan ve bitki dokularında filozinin yaygın varlığını ortaya koydu ve bileşiğin, oksijen varlığında disülfid formuna geri dönüşlü oksidasyona girebilen sistein içerdiği sonucuna varmıştı. 1921 yılında bir doku kas dokusundan çıkarılarak, bunun otomerikleştirilebildiğini ve sistein ile birlikte glutamik asit içerdiğini bildirmişlerdir. Kesin bir kompozisyonun yokluğunda, “geçici olarak, kolay referans için glutatyon isminin kabul edilebilir olacağını” öne sürmüştür .
Hopkins’in glutatyonun glutamik asit dipeptidi olduğunu ve sistein, bileşiğin muhtemelen bir tripeptid olduğu konusunda bir raporla karşı karşıya geldiğini görmüştür . İki yıl sonra, bileşiğin kristalin formda hazırlanması için yeni bir prosedürün geliştirilmesi, glutatyonun gerçekten de bir glutamik asit, sistein ve glisin tripeptidi olduğunu doğruladı . Aynı yıl, Hopkins bunun için ve vitaminler ve ilgili beslenme faktörleri ile ilgili diğer çalışmalar ile ilgili nobel ödülünü aldı.
Bitkilerde glutatyon fonksiyonlarının karakterizasyonuna giden yol, vitaminler üzerinde çalışan başka bir Nobel Ödülü sahibi tarafından açıldı. Szent-Gyorgyi (1931), lahana yaprağı dokusunun, glutatyonun eş zamanlı oksidasyonunu içeren bir işlem olan askorbik asitin oksitlenmiş formunu azaltabildiğini gözlemlemiştir. Aslında, terminal oksidazlar ve oksitleyici katalizörlerin mevcudiyetine rağmen, askorbik asidin bitkilerde neredeyse her zaman indirgenmiş durumda bulunduğunun erken tanınması, bir indirgeme mekanizmasının mevcut olması gerektiği sonucuna yol açmıştır. 1936’da Hopkins ve Morgan, indirgeyici maddenin glutatyon olduğu sonucuna vardılar .
1960’lı yıllarda, süperoksitin keşfi de dahil olmak üzere, reaktif oksijen türlerinin (ROS) biyolojik öneminin giderek daha fazla tanınması, bitkilerde glutatyonun yenilenmiş ilgisini artırdı. Bu, askorbat-glutatyon etkileşimlerinin fizyolojik bir bağlamda dahil edilmesini içerir. Bu nedenle, askorbat-glutatyon yolağına kloroplastlardaki hidrojen peroksit metabolizmasında anahtar bir fonksiyon atanmıştır ve glutatyon genel olarak stres direncinde rol oynamıştır. Aynı zamanda enzim regülasyonunda kloroplast tiyollerin rolleri karakterize edildi.Ardından glutatyon sentezi, bozunması, taşınması ve kompartmantasyonu ile ilgili detaylara dikkat edildi.
Klonlama ve transgenik teknolojinin gelişmesiyle, glutatyonun antioksidan rolünün tanınması, glutatyon içeriği arttırılmış veya indirgeme kapasitesine sahip bitkilerin üretimini gördü .O zamandan beri, Arabidopsis mutantlarının analizi, bitki gelişimi için glutatyonun gerekli olduğuna dair ikna edici gösteriler sağlamıştır . Günümüzde glutatyonun redoks homeostazında ve sinyallemede ve savunma reaksiyonlarında önemli olan bitkilerde çok fonksiyonlu bir metabolit olduğuna dair kesin kanıtlar vardır.
Bu içgörülerden en önemlilerinden bazıları, Arabidopsis mutantlarının ve genomik ve post-genomik yaklaşımların oluşturduğu sürekli büyüyen bilgi gövdesinin mevcudiyeti ile mümkün olmuştur. Birlikte, bu bilgi, bu küçük tiyol bileşiğini, bitki gelişimi ve çevredeki tepkilerin düzenlenmesinin kalbinde yer alır.
1 Kaynaklar ve Yapısı
1.1 Köken ve Kompozisyon
Glutathione (Glutatyon) (γ-L-Glutamil-L-sisteinilglisin), üç diyet amino asidinden oluşan küçük bir tripeptid moleküldür; L-glutamat, L-sistein ve glisin. [1] Bu tripeptit, hücre içindeki oksidatif süreçleri düzenleyen madde olarak bu tripeptidi kullanan ait olduğu sistemden Glutathione (Glutatyon) sistemi dolayı popüler bir antioksidan olarak bilinmektedir. [2] Glutathione (Glutatyon) ayrıca bazı bileşiklerin vücutta birleşmesinde ve onları detoksifikasyon (vücuttaki zehirli maddelerden arınma) bir rol oynamaktadır ve besin supplementi için doğrulama olarak da kullanılmaktadır.[3]
1.2 Kaynaklar ve Yapı (Nerelerde ve Hangi Besinlerde Bulunur)
Glutathione (Glutatyon), dahili bir antioksidan olmanın ötesinde, çoğu gıdadan besin arzında bulunur. Bir çalışma örneğinde ortalama günlük alım 34.8 mg, ancak geniş bir aralık 13-109.9 mg’dır. Diyet Glutathione (Glutatyonun) yarısından çoğu, et kaynaklarından çeyrekten daha az olan meyve ve sebzelerden bulunur. [4] Bununla birlikte, beslenme Glutathione (Glutatyon) içeriği, yaygın Glutatyon aktivitesi ile ilişkili göstermemektedir. [4]
Glutathione (Glutatyon), insan beslenmesinde gıda ürünlerinde bulunur, ancak en üretken diyetlerde bile tüketilen dozlar glutatin veya onun prekürsörü (N-Asetilsistein) ile desteklenerek elde edilenden önemli derecede daha küçüktür. Diyet glutatin genel glutatin aktivitesi ile ilişki göstermez.
1.3 Biyolojik Önemi
Glutathione (Glutatyon), insan vücudunda en tanınmış nonenzimatik antioksidan olarak bilinen ve Glutatyon metabolizmasının düzenlenmesinde rol oynayan bir enzim sistemi için bir madde olan bir tripeptittir (L-glutamik asit, L-sistein ve glisin). [1]
Glutathoine, oksidasyonu düzenleyen ‘Glutatyon sisteminde’ bir ara maddedir.
Y-Glutamil Sistein Sentetaz (GCS) olarak bilinen bir enzim, Glutathione (Glutatyonun) sentezinde, özellikle de glutamat ve sistein birleştirilerek γ-glutamil sistein olarak bilinen bir dipeptit (peptit bağı ile bağlanmış iki amino asit) oluşturmak için birinci reaksiyona neden olan bir glutamat-sistein ligazdır. [5] Bu enzim, bir hücredeki Glutathione (Glutatyon) eylemlerini değerlendiren bazı farmakolojik müdahalelerin bir hedefidir; çünkü Buthionine SulfOximine (BSO) ile bastırarak aktif Glutatyonun tükenmesine yol açabilir [6] ve bu ilaçların etkilerini arttırarak Glutathione (Glutatyon) aktivitesini ve antioksidan etkileri artırabilir. [7] GCS eksikliği hem Glutathione (Glutatyon) da hem de hücresel Glutatyon-S-transferaz aktivitesinde bir azalmaya neden olur. [8] Glutathione (Glutatyon) kendisi bu enzim üzerinde hem bakteri [9] hem de fare hücrelerinde, [11] negatif bir düzenleyici rol oynadığından aşırı aktiviteden Glutathione (Glutatyon) üretiminin fazlalığı muhtemel görünmemektedir.
- Y-Glutamil Sistein Sentetaz (GCS) : Glisin parçalama sistemi (GCS), glisin geri dönüşümlü oksidasyonunu katalize eden P, H, T ve L proteinlerinden oluşan bir çoklu enzim sistemidir.
- Glutamat-sistein ligaz : Kimyasal reaksiyonu katalize eden hücresel glutatyon Glutatyonun biyosentetik yolunun ilk enzimidir.
- Buthionine SulfOximine (BSO) : Glutatyon düzeylerini azaltan ve kanser tedavisinde kemoterapi ile birlikte araştırılan bir sulfoximindir.
- Glutatiyon-S-transferaz : Detoksifikasyon amacıyla ksenobiyotik maddelere indirgenmiş glutatyon formunun birleşimini katalize etme yetenekleri ile bilinen ökaryotik ve prokaryotik faz II metabolik izozimlerin bir ailesini içerir. .
Glutathione (Glutatyonun) sentezinde yer alan ikinci enzim, önceki enzimatik reaksiyonda oluşturulan γ-glutamil sisteini alan Glutatyon sentezidir (ligaz) ve glisin adı verilen tripeptidi oluşturan glisin içermektedir. [12] Bu enzim maya ve bakterilerde bulunur, ancak fare ve insan çeşitleri ile çok az benzerlik gösterirler; fare çeşidi, insan çeşiti ile yaklaşık % 88 homolojiye (kökendeşliğe) sahiptir. [13] [14] [15] Enzim, insanlarda Cys-422’nin işlev görmesini gerektirir [16] ve onun işlevi Methionine SulfOximine (MSO) ile yapılan deneylerde engellemektedir. [17]
- Methionine SulfOximine (MSO) : Memeli hücre dizilerinde plazmid entegrasyonu için bir seçim maddesi olarak yaygın olarak kullanılan güçlü bir glutamin sinetaz aktivitesi inhibitörüdür.
Glutathione (Glutatyon) sentezinin hız sınırlama aşaması, normal koşullar altında her iki enzimin aktivitesi değil, tripeptidi oluşturan amino asitlerin (L-sistein) birinden sağlanması gibidir; [18] Bununla birlikte, bazen Glutathione (Glutatyon) sentezini arttırmak için N-asetilsistein supplementi (N-asetilsistein L-sistein oluşturmak üzere deasetil hale getirildikten sonra) kullanılır. [18]
Vücuttaki Glutathione (Glutatyon) sentezi, bir tanesi gama konfigürasyonunda L-sistein ve glutamik asiti birbirine bağlayan (γ-glutamil sistein üreten) ikinci enzimi sonuçta, Glutathione (Glutatyonu) oluşturmak için bir glisin molekülü ekleyen iki enzimi kapsamaktadır.
Glutathione (Glutatyonun) kendisi hem antioksidan etkilerden önce indirgenmiş Glutathione (Glutatyon) (GSH) olarak bilinen indirgenmiş bir formda hem de hedefler üzerinde antioksidan etkiler bıraktıktan sonra okside bir formda (GSSG) bulunur. İkisi GSH / GSSG oranı oluştururken, GSH / GSSG oranı normalde toplam Glutathione (Glutatyonun) % 98’ini oluşturur ve orandaki değişiklikler, hücresel oksidatif (oksitleyen) dengedeki değişiklikleri belirtir. [19]
- GSSG : Glutatyon disülfid, iki glutatyon molekülünden türetilmiş bir disülfittir. Canlı hücrelerde glutatyon disülfür, koenzim NADPH’den eşdeğerleri azaltarak iki glutatyon molekülüne indirgenir.
- NADPH : Hücre dışı boşluğa bakan hücreye bağlı bir enzim kompleksidir.
Okside olmuş Glutathione (Glutatyon) (GSSG), NADPH’ye bağlı Glutathione (Glutatyon) disülfid redüktaz enzimi [12] vasıtasıyla Glutatyona dönüştürülebilir ve bu enzimin aktivitesi, kısmen Glutathione (Glutatyon) tarafından kontrol edilir. [20] Bu enzimin aktivitesi genel GSH / GSSG oranının önemli bir belirleyicisidir. [12]
- Glutatyon Disülfid redüktaz enzimi : İnsanlarda GSR geni tarafından kodlanan bir enzimdir. Glutatyon redüktaz , glutatyon disülfid (GSSG) ‘nin oksidatif strese karşı koyan ve hücrenin azaltıcı ortamını koruyan kritik bir moleküldür olan sülfhidril formundaki glutatyona (GSH) indirgenmesini katalize eder.
Glutatyon, indirgenmiş form (Glutatyon) ve okside form (GSSG) olmak üzere iki formda bulunur. RGSH’nin GSSH’ye oranı, daha oksidatif bir durumu düşündüren azaltılmış forma (Glutatyona) göre artan okside formlarla (GSSG) birlikte bir hücrenin genel oksidatif durumunun bir göstergesidir.
Antioksidatif etkiler göstermek için Glutathione (Glutatyonu) kullanan antioksidan enzimler, Glutatyon S-transferazlar (GSTs) olarak bilinir ve Glutathione (Glutatyon) molekülünü bir elektron çifti bağışlamaya ve işlemeye hazırlayarak ve bu saldırının mümkün olan hedeflere ulaşmasına izin vererek çalışırlar. Elektronları kabul etmek (elektrofilik hedefler), elektronların transferini sağlar; bu transferin kendisi antioksidan etkisi yapmaktadır. [21]
- Glutatyon S-transferazlar (GSTs) :Detoksifikasyon amacıyla ksenobiyotik maddelere indirgenmiş glutatyon formunun birleşimini katalize etme yetenekleri ile bilinen ökaryotik ve prokaryotik faz II metabolik izozimlerin bir ailesini içerir.
GST enzimleri alfa (α), [22] mu (μ), [23] pi (π), [24] teta (θ), [25] zeta (ζ), [26 ] memelilerinde sekiz ayrı sınıfa ayrılır, sitokromda (solunum sisteminde elektron taşıyıcı) çözünebilir olarak bulunur. GST’lerin iki süper ailesine bölünür, [27] omega (ω) [28] ve hücresel kappa (κ) [29] ve toplu olarak hücreyle İlişkili Proteinler olarak Eicosanoid ve Glutathione (Glutatyon) Metabolizması (MAPEG) olarak bilinen hücresel zarlarla ilişkili olan mikrozomal GST’lerdir. [30]
- MAPEG : Moleküler biyolojide, MAPEG protein ailesi, yüksek ölçüde farklı fonksiyonlara sahip bir hücreyle ilişkili protein grubudur.
- Mikrozom : Ökaryotik hücreler laboratuvarda parçalandığında endoplazmik retikulum (ER) parçalarından yeniden oluşturulan vezikül benzeri yapay dokulardır; Sağlıklı, yaşayan hücrelerde mikrozomlar yoktur.
Başka bir enzim grubu, sekiz bileşiklerden hangisinin araştırıldığına bağlı olarak, farklı etkinlik ve hedeflerle, lipid peroksidasyonunu ve hidrojen peroksidi suya indirgemek için Glutathione (Glutatyon) tripeptidleri kullanan Glutatyon peroksidaz (GPx) enzimleridir. [31] Bu enzimler selenyum bağımlı enzimlerdir ve vücuttaki aktivitesindeki bir azalma selenyum eksikliğinin ters etkilerine aracılık etmektedir. [31] [32]
- Lipid peroksidasyon : Lipit peroksidasyonu lipitlerin oksidatif bozunmasıdır.
- Glutatyon peroksidaz (GPx) : Glutatyon peroksidaz, ana biyolojik rolü organizmayı oksidatif hasara karşı korumak olan peroksidaz aktivitesi olan bir enzim ailesinin genel adıdır.
- Hidrojen peroksidi : Hidrojen peroksit, H ₂O ₂ formülüne sahip kimyasal bir bileşiktir. Saf haliyle, soluk mavi, berrak bir sıvıdır, sudan biraz daha viskozdur.
Glutatin S-transferaz (GST) ve glukoton peroksidaz (GPx) enzimleri, Glutathione (Glutatyonun) birçok antioksidatif etkisine aracılık etmektedir.
Antioksidan etkileri göstermek için enzimleriyle madde olarak Glutatyonun kullanılmasının ötesinde, proteinler üzerindeki L-sistein artıklarını S-glutatiyonilasyon (veya S-glutathiolation) olarak bilinen bir süreçte değiştirebilir. [33] [34] Genel olarak bu işlem proteinlerin hareketlerini değiştirir ve DNA’dan RNA’ya genetik bilginin aktarımını düzenlenmesiyle [35] hem proteinlerin katlanmasına hem de parçalanmasına katılmaktadır. [36] Yaşamsal yolaklar (patikalar) olsa da, bu bilgilerin N-asetilsisteinin Glutathione (Glutatyonun) oral yoldan verilmesinin önemi bilinmemektedir.
Glutathione (Glutatyonun) kendisi klasik antioksidan etkilerinden bağımsız olarak, S-glutatiyonilasyon olarak bilinen bir işlemle protein fonksiyonunu değiştirebilir.
2 Farmakoloji
2.1 Sindirim
Küçük bir peptit molekülü olması nedeniyle Glutathione, enzimin baskın olduğu Oniki parmak bağırsağın sınırında genellikle γ-glutamiltransferaz ile ince bağırsakta hidrolize (sindirime) tabi tutulur. [38] Glutatyonun damardan alımı, çoğunlukla kendini oluşturan amino asitlerle bozunduğundan ve kanda L-sisteini arttırdığından, sindirildikten sonra hidroliz olabilir. [39]
İnsan bağırsak hücrelerinde Glutathione (Glutatyon) emilimi için bir taşıyıcı olduğu görülmektedir [40] ve farelerde ağızdan aldıkları Glutathione (Glutatyon) ile kanda [41] ve dokuda [42] Glutathione (Glutatyon) da artış bildirilmiştir; ancak insandaki genel Glutathione (Glutatyon) aktivitesi ile ilişkilendirilmez. [4]
Diyetle veya oral yoldan alınan Glutathione (Glutatyon), bağırsaklardan ve kanda kendi oluşturucu amino asitlerine hidrolize edilebilir, ancak bazı Glutathione (Glutatyonun) bağırsaklardan sindirim yoluyla dolaşıma girmesi olasılığı vardır.
2.2 Serum
Sağlıklı kişilerde 3gr Glutathione (Glutatyonun) (0.15mM / kg) solüsyonunun oral yoldan tüketilmesi, başlangıçta göreceli olarak 270 dakika boyunca, kan dolaşımdaki Glutathione (Glutatyon) konsantrasyonlarını arttırmada başarısız olmuştur. [43] Glutathione (Glutatyon) damardan alımı, serum L- sistein, Glutathione (Glutatyon) içerisindeki L-sistein miktarına yaklaşık olarak eşdeğerdir; serumdaki Glutathione (Glutatyonun) bozunumunu düşündürmektedir.[39] [44]
Bir çalışmada, sağlıklı insanlarda Glutathione (Glutatyonun) kırmızı kan hücresi depolarını arttırmak için başarısız olan 1000 mg Glutathione (Glutatyonun) oral yoldan kullanımı dört hafta içinde supplement edildiğini göstermiştir. [45] Başka bir çalışmada, test edilen supplement üreticisi Setria® tarafından finanse edilmiş, ancak çelişki bulunamamıştır. Beyan edilen artış,altı ay içinde aynı dozu veya daha az 250 mg’lık bir dozu kullanarak kırmızı kan hücresi Glutathione (Glutatyondaki) artışlar tepe seviyesindeyken % 30-35’e ulaşmıştır; [46] 250 mg, 1.000 mg’a kıyasla altı ayda daha az etkilidir. [46]
Glutathione (Glutatyon) kan içinde stabil değildir ve ister oral veya damariçi uygulama yoluyla olsun, Glutathione (Glutatyon) L-sistein veya diğer kükürt içeren moleküllere kolayca indirgenir. Oral Glutathione (Glutatyonun) vücuttaki Glutatyonu artırdığı hala mümkündür, ancak bu muhtemelen sindirim için L-sisteine indirgenmesini gerektirir.
2.3 Hücresel Kinetik
Glutathione (Glutatyon), hücre içinde olarak sentezlenir ve bir hücreden dışarı akarken, kurucu amino asitlere hidrolize olma eğilimi göstermektedir, daha sonra hücreler tarafından geri alınır ve hücre içi olarak Glutatyona yeniden sentezlenir. [18] γ-glutamil transpeptidaz Glutathione (Glutatyondaki) γ-glutamil bağı, bir başka amino aside, genellikle iki L-sistein molekülünün bir ürünü olan sistin bağlanan bir sistein-glisin dipeptid ve γ-glutamil kısmı üretir. Hücre dışı taşınması ve başka bir dokuya ulaşması üzerine γ-glutamilamino asit dipeptide (iki amino asitten oluşan cisim), amino asidi serbest bırakmak için γ-glutamil siklotransferaz ile bölünür ve 5-oxoprolinaz ile glutamin haline dönüştürülen siklik şekli, glutamik asit (5-oxoprolin) üretir. [48] [18]
- 5-oxoprolinaz : Piroglutamik asit, glutamik asit veya glutaminin serbest amino grubunun bir laktam oluşturmak üzere siklize edildiği, her yerde bulunan az sayıda çalışılmış doğal amino asit türevidir.
Tripeptid olarak bir Glutathione (Glutatyon), bir hücreden akıntının çoğu hücrenin içine sağlam bir şekilde emilemze. Bu, serumda bazal bir Glutathione (Glutatyon) içeriğine yol açar; normal aralık 3.8-5.5μM’dir ve yarılanma ömrünün yaklaşık 14.1 +/- 9.2 dakikalık olduğu kaydedilmiştir. [44] [49] Glutathione (Glutatyon) emilebileceğini kaydeden hücreler hepatositleri (HepG2), [50] bağırsak mukozal hücrelerini ve retinal hücreleri içerir.[51] [52] [53]
- HepG2 : Çok çeşitli kimyasal ve ilaçların toksik etkilerini değerlendirmek için yaygın olarak kullanılmaktadır.
Glutathione (Glutatyon), sentezlendiği hücrelerden ihraç edilebilir ve kanda bir dereceye kadar bozulmamış haliyle bulunur. Bununla birlikte, çoğu hücrenin onu emmek için parçalaması gerekir.
2.4 Faz II Enzim Etkileşimleri
Glutathione (Glutatyon), seçilen Faz II Enzimleriyle diğer moleküllere birleşebilir; bu işlem, klasik olarak bir detoksifikasyon süreci olarak adlandırılır; çünkü bu birleşim molekülü karaciğer ve böbrekler tarafından uzaklaştırılması için etiketler; [54] bazı durumlarda Glutathione (Glutatyon) birleşimi, hedef molekülü biyoaktif hale getirir. [55] Bu süreç, hem ksenobiyotikler (vücudun dışından gelen şeyler) yanı sıra steroidler [56] ve prostaglandinler (kan basıncı üzerine etki eden bileşikler grubu) gibi bazı dahili moleküller için de geçerlidir. [57]
Bu enzimler, Glutathione (Glutatyon) S-transferazlardır (GSTS) ve birleşim reaksiyonu, birleşim sürecinde Glutathione (Glutatyonun) elektrofilik hedeflere nükleofilik bir saldırı (bir çift elektron vererek) yaptığı bir anti-oksidasyon reaksiyonuna benzemektedir. Birleşim sonrasında, karaciğerden hızlı bir şekilde bağırsaklara atılır (böylelikle dışkı metaboliti oluşturur) ve böbreklere giderek nihayetinde merkapturik asit olarak bilinen asetik asit haline getirilmiş bir L-sistein birleşimi olarak idrarla atılır. [54] [55]
Glutathione (Glutatyon), hedefleri birleştirmek için Glutathione (Glutatyon) S-transferaz (GST) enzimleri tarafından kullanılır. Bu birleşim, hedefin yapısını değiştirir ve çoğu durumda bu, vücudun hedefin çıkarılmasına yardımcı olarak zehirin etkisini gidermek için bir rol oynamaktadır ve hedefin eylemlerini / yan etkilerini arttıran birkaç durumla ilişkilendirilir.
3 Kalp ve Damar Sağlığı İle Etkileşimleri
3.1 Kalp Dokusu
Koşu bandı eğitimine tabi olan farelerde, iskemi-reperfüzyondan (IR) önce 17 gün boyunca 5 gr / kg Glutathione (Glutatyonun) oral yoldan alınması, supplementleme koruyucudur. Glutathione (Glutatyon), sol ventrikül sistolik basıncındaki IR kaynaklı artışları ve ayrıca tek başına Glutathione (Glutatyon) ve tek başına egzersizden daha fazla kasılabilirliği (+ dP / dt) düşürmüştür (ki bunların ikincisi koruyucu değildir). [59]
- İskemi-reperfüzyon : Kritik hastalarda önde gelen ölüm nedenlerinden biri olan çoklu organ yetmezliğine yol açabilen miyokard enfarktüsü, transplantasyon, inme ve travmayı takiben sık görülen bir durumdur.
4 İltihaplanma ve Bağışıklık Sistemi
4.1 Virolojik Etkileşimler
HIV’li kişilerin oluşturduğu makrofajlar, enfekte olmayan kontrollerden alınan makrofajlara göre (indirgenmiş Glutathione (Glutatyon)a göre) daha yüksek konsantrasyonda GSSG’ye sahip gibi görünmektedir. [60] Bu, makrofajlarda, HIV enfeksiyonu ile görülen düşük bir glutamin-sistein ligaz (GCLC) ekspresyonuyla ilişkili olduğu düşünülmektedir. [60]
- Makrofaj : Bağışıklık sisteminin, hücresel enkazı, yabancı maddeleri yutup sindiren bir tür beyaz kan hücresidir. Mikroplar, kanser hücreleri ve yüzeyinde sağlıklı vücut hücrelerine özgü protein türlerine sahip olmayan diğer her şey fagositoz olarak adlandırılan bir süreçtir.
HIV ile stabil anti-retroviral tedavide izole edilen ve M. tuberculosis ve 5-10μM glutathione ile kuluçka edilen makrofajlar, azaltılmış Glutatyona (HIV + % 53-93 ve HIV kontrollerinde % 80-83) bir artışa neden olup, sadece bununla eşleştirilmiştir (10 mM’de N-asetilsistein). [60] Potansiyel farklılığı, lipid peroksidasyonunu değerlendirirken (malondialdehid testi ile) ve M. tuberculosis’in hücre içi büyümesinin azaltılmasında devam etmiştir. [60]
- Malondialdehid testi : Biyolojik numunelerdeki femtomol miktarlarında, gaz kromatografisi-kütle spektrometresi ile analiz edilir.
- M. tuberculosis : Mycobacteriaceae familyasında ve tüberkülozun etken maddesi olan bir patojenik bakteri türüdür.
5 Oksidasyon ile Etkileşim
5.1 Süperoksit
Tek bir elektron, bir oksijen molekülü (O 2) tarafından soyutlandığı zaman veya metabolik reaksiyonların yan ürünü olarak üretilen süperoksit (O 2 -), hem N-asetilsistein [62] hem de Glutathione (Glutatyonun) [63 ] olduğu serbest radikaldir. [64] Bu tür reaksiyonlar için hız değişimi zayıf olmasına rağmen (bu nedenle bu durumda düşük potensli antioksidanlardır) doğrudan ve enzimatik olmayan şekilde reaksiyona girmektedir.
Süperoksit oluşumu oksijen molekülünün zarları kolayca kolayca çaprazlama (H 2 O 2 ‘ye benzer, ancak O 2 ‘ye değil) yapabildiği ve oksijen molekülünün metabolik reaksiyonlarda her yerde gerekli olması nedeniyle oksidasyon üretiminde ortak bir ilk safhadır. [61]
Enzimatik antioksidan etkiler (peroksidazlar ve S-transferazlar) uygulamak için, Glutathione (Glutatyonu) kullanan enzimlerin bu radikal üzerinde güçlü bir antioksidan etkiye sahip olmadığı ve oksijen molekülünün dahili salgılanması süperoksit dismutaz enzimlerinin (SOD) işleyeceği eğilimi taşıyor. [66] [67]
- SOD : Süperoksit radikalinin değişimini sıradan moleküler oksijen veya hidrojen perokside dönüşümlü olarak katalize eden bir enzimdir.
- H2O2 : Hidrojen peroksit, H ₂O ₂ formülüne sahip kimyasal bir bileşiktir. Saf haliyle, soluk mavi, berrak bir sıvıdır, sudan biraz daha viskozdur. Hidrojen peroksit en basit peroksittir.
Süperoksit (O 2 -), hücrede oksidatif etkiler yapabilen temel serbest radikallerden biridir ve genellikle süperoksit dismutaz enzimi tarafından işlenir; bu enzim hidrojen peroksit haline dönüştürür ve sonra Glutatyonu azaltır; Glutathione (Glutatyon) ve enzimlerinin, doğrudan Süperoksit’i azaltmada fazla antioksidan potansiyeli yoktur.
5.2 Hidrojen Peroksit
Süperoksit radikali, süperoksit dismutaz (SOD) ile hidrojen peroksit (H2O2) ‘ye dönüştürülür ve bu oluştuğunda, Glutathione (Glutatyon) peroksidaz enzimi (GPx), iki Glutathione (Glutatyon) tripeptid (ve oluşumu) kullanılarak H2O ‘ya indirgeyebilir. [68] H2O2 ayrıca aerobik metabolik reaksiyonlarda bir yan ürün olarak da üretilebilir. [61] [69]
Antioksidan enzim katalaz, ayrıca H2O2 ‘yi su ve oksijene ayrıştırarak giderir. [70] H2O2‘nin yüksek konsantrasyonlarda katalazı inaktive edebileceğinden, [71] [72] bu inaktivasyonun GPx’e karşı korunduğu görülmektedir; Katalaz ve GPx birlikte hareket eder. [73]
GPx enzimleri tarafından kullanılan Glutathione (Glutatyon), hidrojen peroksit (H2O2) olarak bilinen oksidanın potansiyel birikimlerinin azaltılmasında katalazın yanında bir role sahiptir. Bu enzimler, hidrojen peroksiti suya (veya katalaz durumunda su ve oksijen) geri döndürebilir.
5.3 Hidroksil
Hidroksil radikali (OH •, OH- olan nötr formdaki hidroksi), oksijen molekülü- bir Fenton reaksiyonu yoluyla demir ile reaksiyona girdiğinde üretilen güçlü bir radikaldir ve hafif ve tersinir (kimyasal, fiziksel ve mekanik dönüşüm) oksidanlar olan oksijen molekülü – ve H2O2‘den farklı olarak OH protein yapılarının geri döndürülemez bir düzenleyici malzemesidir. [74] Hidroksilin, sonraki DNA hasarı gibi bir hücredeki artan H2O2 konsantrasyonlarının daha olumsuz etkilerinin çoğuna aracılık ettiği düşünülmektedir. [75] [76]
- Fenton Reaksiyonu : Fenton 1894’te, birkaç metalin hidrojen peroksit kullanımını geliştiren özel bir oksijen transfer özelliğine sahip olduğunu keşfetti. Aslında, bazı metaller yüksek oranda reaktif hidroksil radikalleri üretmek için güçlü bir katalitik güce sahiptir.
6 Vücut Organları İle Etkileşimi
6.1 Bağırsaklar
Ülseratif kolit [77] ve Crohn hastalığı da dahil olmak üzere iltihaplı bağırsak hastalıkları, [78] oksidatif stres artışı ve aynı anda Glutathione (Glutatyon) konsantrasyonları gibi oksidatif savunmaların azalması ile karakterizedir. [79] Glutathione (Glutatyon) bağırsaklardaki dokudaki temel nonenzimatik antioksidandır. [80] Glutathione (Glutatyonu) koruyan önlemler bu hayvan hastalığının, hayvan modellerinde iltihaplanmayı ve oksidatif stresini azaltma eğilimindedir. [81] Glutathione (Glutatyon) terapötik bir madde olarak araştırılmıştır.
Farelerde, trinitrobenzen sülfonik asit (TNBS) vasıtasıyla kolit indüksiyonundan bir saat önce bir Glutathione (Glutatyon) (200 mg / kg) enjeksiyonu, tuzdan koruyucu etkiler ortaya koyarken, kolitten 8 hafta boyunca günde 50 mg / kg Glutathione (Glutatyon) (enjeksiyon) uyarıldığı görülmüştür. Lipid peroksidasyonu ve iltihaplanmadaki değişiklikleri hemen hemen abarttığını belirtmiştir. [82]
- TNBS : Mekanizması ve tedavisi üzerindeki çalışmalar için iltihaplı bağırsak hastalığını (IBD) / kolonik iltihabını indüklemek için kullanılır.
- Lipid peroksidasyon : Lipit peroksidasyonu lipitlerin oksidatif bozunmasıdır.
İnsanlarda mesalamin tedavisi uygulanır ve daha sonra 800 mg N-asetilsistein Glutatyon düzeylerini geri kazandırabilir veya plasebo verildiğinde, kombinasyon tedavisiyle koruyucu etki hem hafif hem de istatistiksel olarak anlamlı bir değere ulaşamamıştır. [83]
6.2 Erkek Cinsel Organı
Erkek kısırlığı, genel olarak antioksidanların muhtemel bir terapötik rolünü ima eden aşırı oksidatif stres ile karakterize bir durumdur. [84] Özellikle bir Glutathione (Glutatyon) peroksidaz eksikliği (selenyum eksikliği nedeniyle, enzim bunu gerektirir), erkek dölleme hücresinin orta parçasını (başı kuyruk arasındaki bölüm) etkileyerek bozuk hareketlilik ve morfolojiye neden olur gibi görünmektedir. [85] [86]
Glutathione (Glutatyonun) terapötik etkisi, 600 mg Glutathione (Glutatyonu) damarda enjeksiyon olarak kullanan bir çalışmada doğrulanmış; bu, geliştirilmiş sperm hareketliliğine vermiştir. [87] Kısıra yakın (üreme yeteneği zayıf) erkeklerde üç aylık periyot boyunca bu özgül fayda (geliştirilmiş hareketlilik), laboratuvar ortamında N-asetilsistein ve 600 mg NAC ile günlük olarak kaydedilmiştir. [88] [89]
Glutathione (Glutatyon) enjeksiyonu, spermlerin morfolojisini ve hareketliliğini arttırarak erkek kısırlığını (döllenebilirlik, verimlilik) artırabilir. Bu etki, N-asetilsisteinin oral yoldan ilave edilmesini kullanan ön araştırmalarda da belirtilmiştir; bugüne kadar Glutathione (Glutatyonun) oral yoldan verilmesine ilişkin herhangi bir çalışma yapılmamıştır.
7 Uzun Ömürlülük ve Hayatı Uzatma
7.1 Gerekçe
Hastalığın bulunmadığı durumlarda bile yaşlanma sürecinde hücrelerde, Glutathione (Glutatyon) içeriği azaltılır ve daha oksidatif bir duruma neden olur. [90] [91] [92] [93] En azından yaşlı farelerde bunun nedeni, γ-glutamil transpeptidaz ile metabolizma üzerinde herhangi bir değişiklik yapmadan veya Glutathione (Glutatyon) sentezinin ikinci basamağının (Glutatyon sentezinin katalize ettiği) sentetik kapasitelerinin azalmasıyla ilişkili olduğu görülmektedir. Glutatyon redüktaz tarafından bir antioksidandır, [94] ancak bu mekanizma insanlarda araştırılmamıştır.
Bununla birlikte, yaşlı insanlarda Glutathione (Glutatyon) sentez oranının (fraksiyonel ve mutlak) gençlik kontrollerine göre daha düşük olduğu tespit edilmiştir. [95] Bu azalma Glutathione (Glutatyon) sentezinde kullanılmak üzere glisin ve sistein havuzlarını azaltacak yaşlanmada görülen tüm vücut protein döngüsünde bir azalma ile ilişkili olabilir. [96] [97] [95] Gerçekten de, kırmızı kan hücresi, Glutathione (Glutatyon) düzeyleri ve ayrıca L-sistein ve glisin içeren amino asitler (glutamat değil) yaşlılarda gençlere oranla azaldığı ve [95] N- asetilsistein (100 mg / kg L-sistein) ve glisin (100 mg / kg). Glutathione (Glutatyon) konsantrasyonlarını iki haftalık geri yükleme seviyelerinde % 94.6, Glutathione (Glutatyonun) gençlerde görülen sentez oranlarını geri yüklediği kaydedilmiştir. [95]
Bununla birlikte, diyet proteinini sınırlandırarak sağlıklı yaşlı olmayan erişkinlerde, azaltılmış Glutathione (Glutatyon) sentezi veya dönüşümü ya da sadece diyet proteininde bulunan kükürt içeren amino asitleri uyarabildiğinden , yetersiz beslenme alımı, aynı zamanda Glutathione (Glutatyon) düzeylerini düşürebilir. [98] [99]
Glutathione (Glutatyon), belirgin hastalık durumu olmasa bile, genç kontrollerle karşılaştırıldığında yaşlılarda azalmış gibi gözükmektedir. Oral olarak, Glutathione (Glutatyonun) öncü amino asitlerini (L-sistein ve glisin) sindirerek, Glutathione (Glutatyon) seviyelerini genç kontrollerde oldukça hızlı bir şekilde geri getirebilir.
8 Diğer Tıbbi Durumlar
8.1 Otizm
Otizm, malondialdehit (MDA) [100] gibi yükselmiş oksidatif metabolitler ile ilişkili olduğu için, Glutathione (Glutatyon) metabolizması araştırılmış ve ceruloplasmin ve transferrin gibi mineral-şelatlayıcı proteinlerin azaltılması, bilinen serbest minerallere yol açmıştır. Oksidatif strese katkıda bulunmak için, [101] otistik çocukların genel vücut durumunun antioksidanstan daha fazla pro-oksidatif olduğunu önermektedir. [102]
- Malondialdehit (MDA) : Aslında MDA, 1980’lerde MDMA’nın bir sokak ilacı olarak ortaya çıkmasına kadar orijinal “aşk ilacı” idi. MDA için onaylanmış tıbbi kullanım bulunmamaktadır.
- Ceruloplasmin : İnsanlarda CP geni tarafından kodlanan bir ferroksidaz enzimdir. Ceruloplazmin, kandaki başlıca bakır taşıyıcı proteindir ve ek olarak demir metabolizmasında da rol oynar.
- Transferrin : Kanın demire bağlandığı ve vücut boyunca taşıdığı ana proteindir. Bir transferrin testi direkt olarak kandaki seviyeyi ölçer.
Plazma Glutathione (Glutatyon) ve azaltılmış biçimi [103] [104] [105] otistik çocuklarda kontrol ile ilişkili olarak düşüktür ve oksidize Glutathione (Glutatyon) daha yüksektir. [106] Glutathione (Glutatyon) peroksidazın karışık deliller (bastırılmış ve her ikisi de belirtilmiş ve yükselmiş olsa da) [107] ve GSSG: Glutatyon oranı (genellikle gösterge niteliği taşımaktadır), [108] otistik çocuklar ve kontroller arasında Glutathione (Glutatyon) redüktaz aktivitesinde herhangi bir değişiklik yoktur. [105] Glutathione (Glutatyon) redüktaz aktivitesinin [19] yükseldiği ve daha fazla oksidasyona işaret ettiği gösterilmiştir.
Otizm, genel olarak, otistik olmayan kontrollere göre aşırı oksidatif stres ile karakterize bir durumdur. Glutathione (Glutatyon) vücuttaki ana anti-oksidan sistem olduğu için, bütün vücut antioksidan statüsündeki bozulma, otistik çocuklarda kontrollere göre daha az aktif görünen Glutathione (Glutatyon) sistemine kadar uzanmaktıdır.
Otistik çocuklarda, oral (artan dozlarda günde iki kez 13 kg vücut ağırlığına göre 50-200 mg lipid çözünür glutatyon) veya transdermal (artan dozlarda üç bölünmüş dozda 135-405 mg) kullanılan bir çalışma, Glutathione (Glutatyon) supplementi, her iki tedavide de toplam Glutatyonda anlamlı artışlar kaydetmiştir. Oral grubun serumunda indirgenmiş Glutathione (Glutatyon) da bir artış; çalışmada, başlangıçtaki otistik şiddeti ölçürken, ölçüm tedavi sonrası tekrar edilmemiştir. [49]
9 Besin-Supplement Etkileşimleri
9.1 Alfa-Lipoik Asit
Alfa-lipoik asit (ALA), oktanoik asitten mitokondrilerde üretilen ve hem REDOX antioksidan (hem okside hem de indirgenmiş formda) ve mitokondriyal enzimatik kofaktör olarak kullanılan bir antioksidan tiyoldur. [109] Bir kükürt içeren antioksidan olmakla birlikte Glutathione (Glutatyon) ile benzerlikler paylaşmasına rağmen, Glutathione (Glutatyonun) aksine, bağırsaklardan bozulmadan sindirilir ve vücudu besin supplementi olarak etkileyebilir. [110]
- REDOX : Atomların oksidasyon durumlarının değiştirildiği kimyasal bir reaksiyondur. Bu tür herhangi bir reaksiyon, hem bir indirgeme sürecini hem de tamamlayıcı bir oksidasyon işlemini, elektron transfer işlemleriyle ilgili iki anahtar kavramı içerir.
ALA’nın, Glutathione (Glutatyon) sentezini teşvik etmede bir rolü olduğu görünmektedir. Glutathione (Glutatyon), hücreler arasında bozulmadan aktarılmaz; bunun yerine L-sistin Glutathione (Glutatyon) sentezi için L-sistein sağlamak üzere hücreler arasında taşınır. [18] L-sistin, L-sistein’in (iki okside L-sistein molekülünün birbirine bağlı olduğu) oksidatif bir ürünü olduğundan, ALA, L-sistini iki L-sistein amino asidine indirgeyebilir ve bu nedenle, öncüsünü serbest bırakarak, Glutathione (Glutatyon) sentezini artırabilir. [ 111] Glutathione (Glutatyon) sentezinde hız sınırlayıcı adım için gerekli maddedir .[18]
Ayrıca, GSSG (oksitlenmiş Glutathione (Glutatyon) formu), indirgenmiş alfa-lipoik asit [112] yoluyla doğrudan Glutatyona indirgenebilir ve bu oksidize formuna (dihidrolipoik asit) dönüşür. Glutathione (Glutatyon) aktivitesindeki ALA’nın bu genel destekleyici rolü, çeşitli hücre hatlarında kaydedilmiştir ve farelerde 16 mg / kg ALA ile laboratuvar ortamında gerçekleştiği görülmektedir. [113][114]
Alfa-lipoik asit, oksidize Glutathione (Glutatyon)’u azaltarak, bir hücredeki Glutathione (Glutatyonun) hareketlerini arttırır ve korur.
9.2 Sitrülin
L-sitrulin, nitrik oksit (NO) seviyelerini arttırmak için sıklıkla kullanılan bir amino asittir, güçlü bir damar genişletici ve egzersiz öncesi supplement ile popüler hedeftir. NO oluşturmak için, L-arginin nitrik oksit sentaz (NOS) enzimi tarafından oksijen ile birleştirilir. L-arginin ile ilgili problem, oral yoldan yuttuktan sonra, karaciğerde kan dolaşımına başlamadan önce önemli miktarda parçalanmasıdır. L-sitrülin, NO sentezinin arginin-sitrülin döngüsü yoluyla arginin içine dönüştürülebilen bir yan ürünüdür. [115] Bu nedenle, L-sitrulin, kanda L-arginini artırmak için daha verimli bir yoldur. [116]
- NOS : L-arginin’den nitrik oksit üretimini katalize eden bir enzim ailesidir. NO önemli bir hücresel sinyal molekülüdür.
- cGMP : Döngüsel AMP’ye benzeyen ikinci bir haberci gibi davranır. En muhtemel etki mekanizması, hücresel-geçirgen olmayan peptid hormonlarının dış hücre yüzeyine bağlanmasına yanıt olarak hücre içi protein kinazların aktivasyonudur.
Glutathione (Glutatyonun) NO sinyalini güçlendirebileceğini incelemek için, insan randomize, kontrollü bir çalışmada 200 mg / gün Glutathione (Glutatyonun) yanında 2 g / gün L-sitrulin kullanıldığı test edilmiştir. [116] Artmış cGMP düzeyleri gözlemlense de istatistiksel olarak anlamlı olmamasına rağmen, sitrulin ve Glutathione (Glutatyon) kombinasyonu nitrat ve nitrit düzeylerini tek başına sitrulin’den daha fazla arttırmıştır. Nitrat ve nitrit, NO sentezinde madde ve nitrik oksit yolağının artmış aktivitesi için belirteçler olduğu için, L-sitrulin ve Glutathione (Glutatyon) supplementinin nitrik oksit üretimini tek başına L-sitrulin’den daha fazla teşvik edebileceğini göstermiştir. [116]
Sitrulin ile birlikte Glutathione (Glutatyon) almak, nitrik oksit (NO) sinyalizasyonunu güçlendirebilir. Bunun gerçekleştiği mekanizma henüz net değildir, ancak Glutathione (Glutatyon) varlığına bağlı olarak kan dolaşımında nitrik oksitin uzun süre yaşamasını gerektirebilir.
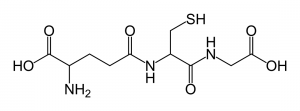
Moleküler Formül: C10H17N3O6S
Moleküler Ağırlık: 307.321 g / mol
Bilimsel Destek ve Referans Metni
Glutathione (Glutatyon) Referanslar
- Glutatyon metabolizması ve sağlık için etkileri .
- Hücre sinyali ve glutatyon redoks sistemi .
- Hücresel glutatyon ve tiyol metabolizması .
- İnsanlarda diyet glutatyon alımı ve alım ile plazma total glutatyon seviyesi arasındaki ilişki .
- Glutatyon sentezinin enzimleri: gama-glutamilsistein sintetaz .
- Buthionine sulfoximine ile glutatyon tükenmesi farelerde DNA delesyonlarını indükler
- Geliştirilmiş gamma-glutamilsistein sentetaz aktivitesi, ilaca bağlı oksidatif stres seviyelerini ve sitotoksisiteyi azaltır .
- Eritrosit glutatyon sentetaz eksikliği sadece glutatyona değil aynı zamanda glutatyon-S-transferaz eksikliğine de yol açar .
- Glutatyon ile nonallosteric geri besleme inhibisyonu ile gama-glutamil-sistein sintetazın düzenlenmesi .
- Gamma-glutamilsistein sintetazın aktif bölgesi tiyolünde: kataliz, inhibisyon ve regülasyon ile ilişkiler .
- İnsan karaciğer gama-glutamilsistein sintetazı için tam uzunlukta bir cDNA’nın klonlanması ve nükleotid dizisi .
- Glutatyon: biyosentez ve modülasyona genel bir bakış .
- Schizosaccharomyces pombe’nin glutatiyon sentetazının büyük alt-birimini kodlayan genin klonlanması ve dizilemesi .
- 2.0 A çözünürlükte Escherichia coli B’den glutatyon sentazının üç boyutlu yapısı .
- İnsan glutatiyon sentetazı için bir cDNA’nın dizilimi ve ekspresyonu .
- İnsan glutatyon sentazında gerekli bir sistein kalıntısının tanımlanması .
- Glutamin ve gama-glutamilsistein sentetazlarının, konvülsiyonları indükleyen metionin sülfoksimin alfa-alkil analogları ile diferansiyel inhibisyonu .
- Sentezinin inhibisyonu ve bunun tersi ile üretilen glutatyon eksikliği; Araştırma ve terapi uygulamaları .
- Oksitlenmiş / azaltılmış glutatyon oranının ölçülmesi .
- Glutatyon disülfid reduktazın glutatyon tarafından inhibisyonu .
- Glutatyon transferazları .
- Selenyum durumu, diyet glukozinolat alımı ve serum glutatyon S-transferaz a aktivitesinin benign prostat hiperplazisi riski üzerine etkileri .
- Glutatyon transferaz mu 2, glioblastoma hücrelerini, otofaji ve lizozom disfonksiyonunu önleyerek amino krom toksisitesine karşı korur .
- Murin Retinada Glutatyon S-Transferaz Pi İzoformu (GSTP1) İfadesi Gelişimsel Olgunluk ile Artar .
- Memeli sınıf teta GST ve karsinojenlere karşı duyarlılık: bir gözden geçirme .
- Zeta, bitkilerden insanlara çeşitli türlerde yeni bir glutatyon transferaz sınıfı .
- Glutatyon S-transferaz polimorfizmleri ve biyolojik sonuçları .
- Glutatyon S-transferaz sınıfı Kappa: sıçan mitokondriyal GST’nin klonlanması ve bir insan homologunun tanımlanması ile karakterizasyon .
- İnsan Kappa sınıfı glutatyon transferazın modelleme ve biyoinformatik çalışmaları, prokaryotik 2-hidroksikromen-2-karboksilat izomerasına benzerlik gösteren yeni bir üçüncü glutatyon transferaz ailesini öngörmektedir .
- MAPEG’in yaygın yapısal özellikleri – eikozanoid ve glutatyon metabolizmasında oldukça farklı işlevlere sahip membran ilişkili proteinlerin yaygın bir süperfamilyası .
- Glutatyon peroksidazları .
- Glutatyon peroksidazlar ve redoks regüle transkripsiyon faktörleri .
- Oksidatif ve nitrozatif strese yanıt olarak S-glutatiolasyon ile protein fonksiyonunun düzenlenmesi .
- Protein fonksiyonunun korunması, restorasyonu ve regülasyonunda glutatiolasyonun rolü .
- Reaktif oksijen türleri tarafından modüle edilen glutatyon redoks potansiyeli, kloroplastta Rubisco büyük alt ünitesinin çevirisini düzenler .
- Protein yıkımının redoks kontrolü .
- Diyet glutatyonun kaderi: gastrointestinal sistemde tutulum .
- sıçan bağırsağındaki gama-glutamil transpeptidaz: lokalizasyon ve amino asit transportunda olası rol .
- Erişkin insanlarda intravenöz glutatyon infüzyonuna yanıt olarak plazma metionin ve sistein kinetiği .
- İnsan ince bağırsak epitel hücrelerinde glutatyon taşıma sistemi .
- Diyet glutatyonunun biyoyararlanımı: plazma konsantrasyonuna etkisi .
- Oral glutatyon doku glutatyon laboratuvar ortamını arttırır .
- Oral glutatyonun sistemik kullanılabilirliği .
- İnsanda yüksek doz intravenöz glutatyon. Plazma ve idrarda kist (e) ine farmakokinetiği ve etkileri .
- Oral Glutatyon takviyesinin insan gönüllülerde sistemik oksidatif stres biyobelirteçler üzerine etkileri .
- Glutatyonun vücut depoları üzerinde oral glutatyon takviyesinin randomize kontrollü çalışması .
- Gama-glutamil transpeptidaz tarafından katalize edilen hidroliz ve transfer reaksiyonları; ayrı substrat siteleri ve L-sistinin yüksek afinitesi için kanıt .
- Gama-glutamil döngüsü: amino asitler için olası bir taşıma sistemi .
- Otizm spektrum bozukluklarında klinik bir glutatyon desteği çalışması .
- Hep G2 hücrelerinde intakt glutatyonun çift yönlü membran transportu .
- Bağırsak mukozasındaki oksidan maruziyetinin tiyol durumu üzerine etkisi .
- Kültürlü insan retinal pigment epitel hücreleri tarafından iki yönlü glutatyon taşınması .
- Sıçan mercek epitelinde yeni, sodyum bağımlı, indirgenmiş glutatyon taşıyıcısının tanımlanması
- Glutatyon analizi: Redoks ve detoksifikasyondaki etkileri .
- Biyoaktivasyon reaksiyonu olarak glutatyon konjugasyonu .
- Sıçan karaciğer glutatyon S-transferaz, izozim 1-1, steroid afinite etiketi, 3 beta- (iyodoasetoksi) dehidroisoandrosteron ile non-substrate steroid bağlanma yeri belirlenmesi .
- İnsan glutatiyon S-transferazları A1-1, A2-2, M1a-1a ve P1-1 ile katalizlenen prostatlandin A2 ve prostaglandin J2’nin glutatyon ile stereoselektif konjugasyonu .
- Glutatyon S-transferazlarının özlü incelenmesi ve toksikolojiye olan önemi .
- Glutatyon takviyesi ve eğitimi iskemi-reperfüzyon laboratuvarına miyokardiyal direnci artırır .
- Glutatyon takviyesi, HIV’de makrofaj işlevlerini geliştirir .
- Süperoksit ve hidrojen peroksite karşı hücresel savunma .
- Süperoksit radikalinin N-asetilsistein ile reaksiyonu .
- Süperoksitin indirgenmiş glutatyon ile reaksiyonu .
- Süperoksit radikali ile tiyol oksidasyon mekanizması .
- Tiyakoid membranların oksijen geçirgenliği: elektron paramanyetik rezonans spin etiketleme çalışması .
- Süperoksit dismutazları – metal ilişkili mekanik varyasyonların gözden geçirilmesi .
- Süperoksit dismutazların kimyası ve biyokimyası .
- Glutatyon peroksidaz ailesi – evrimsel bir bakış .
- Escherichia coli’nin aerobik solunum zinciri ve sülfit redüktaz kompleksinde süperoksit ve hidrojen peroksit oluşumunun primer bölgelerinin belirlenmesi .
- Mitokondriyal katalaz ve oksidatif hasar .
- Tersine çevrilebilir inhibisyon ve hidrojen peroksit varlığında katalazın geri döndürülemez inaktivasyonu .
- Sığır karaciğer katalazının hidrojen peroksit ile intiharının “intihar substratı” için kinetik parametrelerinin belirlenmesi .
- Glutatyon peroksidaz-katalaz kooperatifliği, olgun sıçan oligodendrositleri tarafından hidrojen peroksite karşı direnç için gereklidir .
- Hücre büyümesi ve farklılaşması sırasında hücre içi haberciler olarak reaktif oksijen türleri .
- Fe2 + aracılı fenton reaksiyonları ile sekansa spesifik DNA bölünmesi olası biyolojik etkilere sahiptir .
- Toxic DNA damage by hydrogen peroxide through the Fenton reaction laboratuvar ortamında and laboratuvar ortamında.
- Kolon mukozasının glutatyon içeriği: aktif ülseratif kolitte oksidatif hasar için kanıt .
- Crohn hastalığında glutatyon metabolizması .
- İnflamatuar bağırsak hastalığının mukozasında artan oksidatif stres ve azalmış antioksidan savunmalar .
- Glutatyonun gastrointestinal sistemdeki rolü: bir gözden geçirme .
- Glutatyon düzeylerinin yenilenmesi, deneysel akut kolitte mukozal fonksiyonu iyileştirir .
- Glutatyon takviyesi, deneysel kolitte oksidatif hasarı artırır .
- Ülseratif kolit tedavisinde mesalaminle kombine N-asetil-L-sistein: randomize, plasebo kontrollü pilot çalışma .
- Besin desteği: erkek fertilitesini dört kat arttırmak .
- Selenyum ve hayvanlarda doğurganlık ve insan-bir gözden geçirme .
- Sperm olgunlaşması sırasında selenoprotein PHGPx’in ikili işlevi .
- Erkek infertilitesinde plasebo kontrollü, çift kör, glutatyon tedavisinin çapraz denemesi .
- N-asetil-L-sisteinin insan spermindeki reaktif oksijen türlerine karşı temizleyici etkisi: erkek faktörü infertilitesi için olası bir tedavi yöntemi .
- N-asetilsisteinin semen parametrelerine ve oksidatif / antioksidan durumuna etkileri .
- Sağlıklı yaşlanan yetişkinlerde düşük kan glutatyon seviyeleri .
- İnsan eritrositlerinin glutatyon içeriği, glutatyon redüktaz ve glutatyon peroksidaz aktivitesi ile yaşa bağlı değişiklikler .
- Glutatyon redoks sistemindeki yaşa bağlı değişiklikler .
- Yaşlanma sırasında glutatyon redoks durumundaki pro-oksidan değişim .
- Azalmış sentetik kapasite, Fisher 344 sıçanlarında glutatyon içeriğinde yaşa bağlı düşüşün altındadır .
- Glutatyonun eksik sentezi yaşlanmada oksidatif stres altındadır ve diyet sistein ve glisin takviyesi ile düzeltilebilir .
- Sağlıklı yaşlılarda tüm vücut protein döngüsü .
- Protein gereksinimleri ve yaşlanma: metabolik talep ve kullanım verimliliği .
- Sağlıklı yetişkinlerde güvenli miktarda diyet proteini tüketen eritrosit glutatyon sentezi .
- Kükürt amino asitsiz diyet alan sağlıklı yetişkinlerde kan glutatyon sentezi oranları .
- Otizmde oksidatif stres: artmış lipid peroksidasyonu ve serum seviyelerinde seruloplazmin ve transferrin – antioksidan proteinler .