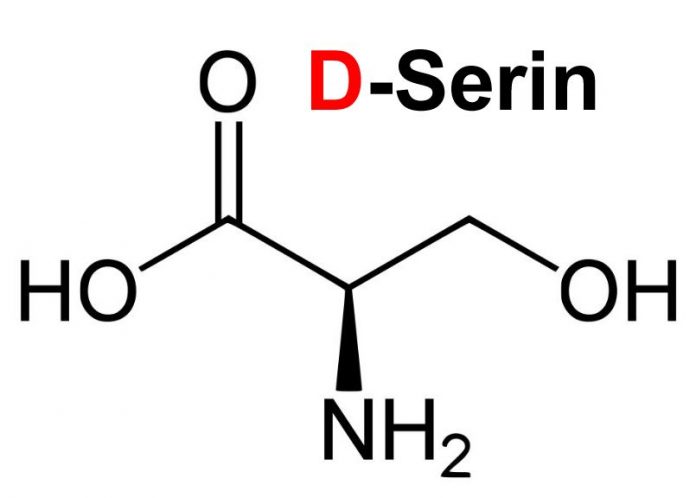
D-Serin Nedir Ve Ne İşe Yarar ?
D-Serin bilişsel iyileştirme ve şizofreni tedavisinde rol oynayan bir amino asittir.
Özet
Tüm Temel Faydalar / Etkiler / Gerçekler ve Bilgiler
D-Serin beynin içinde bulunan bir amino asittir. Glisinden türetilen d-serin, nöronların aktivitelerini düzenleyen bir sinir düzenleyicisidir. D-Serin takviyesi bilişsel düşüş belirtilerini azaltabilir. Aynı zamanda kokain bağımlılığı ve şizofreniyi de içeren azaltılmış N-metil-D-aspartat (NMDA) sinyalizasyonuyla karakterize edilen hastalık belirtilerini azaltabilir.
D-Serin’in şizofreni üzerindeki etkisi iyi araştırılmıştır ve vaat ettiği halde, güvenilmezdir, zira d-serin, takviyeden sonra daima kana ulaşmaz. Saroksin daha güvenilir bir tedavi olabilir.
D-Serine NDMA reseptörlerinde bir koagonisttir, bu da reseptöre bağlanan diğer bileşiklerin etkilerini geliştirdiği anlamına gelir. Bu bileşikler kendiliğinden glutamat ve NMDA içerir. D-Serin genellikle bir nootropik olarak sınıflandırılır.
Bilmen Gerekenler
Şaşırmayın
Glisin veya Sarcosine (mekanizmalarda benzer), Phosphatidylserine (L-serin içeren bir fosfolipid)
D-Serin Bir Formudur
Bilişsel İşlev ve Beyin Sağlığı
Amino asit takviyesi
D-Serin Nasıl Kullanılır Ve Kullanımı Nedir ?
D-serin çalışmalarında kullanılan olağan doz 30 mg / kg vücut ağırlığıdır. Bu 70-90 kilo arasında insanlar için 2,045 – 2,727 mg’lık bir yaklaşık dozaj aralığı ile ilişkilidirler. Bu doz, çeşitli hastalıklardan mustarip insanlarda bilinci geliştirmek için asgari etkili doz olarak görünmektedir.
Ön kanıtlar dozajın sırasıyla 60 mg / kg ve 120 mg / kg’a iki kat artmasının şizofreni hastalarına ek yararlar sağlayacağını öne sürüyor.
| KANIT DÜZEYI | SONUÇ | NOTLAR | ||
|---|---|---|---|---|
| Biliş | Şizofreni semptomlarını azaltmaya bağlı olarak bilişsel performansda bir iyileşme olabilir ve mekanik olarak makul bir olasılık söz konusuyken, bunun normal kontrollerde de çalışabileceği henüz gösterilmedi | |||
| Şizofreninin Belirtileri | D-Serin takviyesi, 30-120 mg / kg arasında doz bağımlı bir şekilde şizofreni semptomlarını (pozitif olmaktan ziyade negatif ve bilişsel belirtiler üzerinde daha fazla etkinlik) azaltabilir, ancak muhtemelen kan D-serindeki güvenilmez artışlara olan faydalarından yararlanmaktadır | |||
| Kaygı | Testten 2 saat önce alındığında, 2.1 g D-serin, sağlıklı insanlarda test sırasında anksiyete azaltılmasında etkili gözükmektedir | |||
| Dikkat | CPT-IP ile değerlendirildiğinde, testten önce 2.1 g D-serin verilen başka sağlıklı kişilerde bilişsel test sırasında sürekli dikkat artmıştır. | |||
| Öznel İyi Olma | Bilişsel testler sırasında bildirilen üzüntü, D-serin desteğiyle plaseboya kıyasla azalmış gibi gözükmektedir | |||
| Parkinson Hastalığının Belirtileri | Ön kanıtlar, D-Serinin standart dozajının Parkinson hastalığının bazı semptomlarını hafifletebileceğini ileri sürmektedir | |||
| Travma Sonrası Stres Bozukluğunun Belirtileri | PTSD’li hastalarda 20mg / kg D-serin kullanan bir çalışma, plaseboya kıyasla takviye ile yarar sağladığını belirtti. | |||
| Çalışan bellek | Testten 2 saat önce 2,1 g ilave edildiğinde hemen geri hatırmada D-serinden yükseltilmiş gibi gözükmektedir. | |||
| Reaksiyon süresi | 2.1 g D-serin, bilişsel testten iki saat önce alındığında, plaseboya kıyasla reaksiyon süresinde bir artış olduğu görülmemektedir | |||
| Serum BDNF | Aksi halde sağlıklı insanlarda 2.1g D-serin, serum BDNF konsantrasyonlarını şiddetle etkilemez | |||
| Sözel akıcılık | Bir kategori akıcılık testinde, iki saat önce alınan 2.1 g D-serin akıcılığı artırmak için görünüyor. Artış plaseboya göre daha büyüktü, ancak iki grubun karşılaştırılması D-serin ile plaseboya göre istatistiksel olarak anlamlı bir yarar sağlamadı |
1 Kaynaklar ve Yapı
1.1 Kaynaklar
D-Serin’in , bir sinirden diğerine geçişi desteklemek için glial (sinir hücreleri) hücrelerde üretilen ve insan vücudunda biyolojik açıdan önem taşıyan ilk D-izomer amino asitlerden biri olan glial hücreden türetilmiş bir sinir düzenleyicisi olduğu bilinmektedir (kısa süre sonra D-Aspartik Asit izledi). [ 1] Glial hücrelerden kaynaklandığı için, bazen bir gliotransmitter veya glio-düzenleyicisi denir. [1] D- Serin, ilk olarak 1865 yılında Emil Cramer tarafından ipek proteinden, özellikle zengin bir kaynaktan elde edildi.
D-Serin, NMDA reseptörlerinin glisin bağlanma bölgelerindeki dahili bir atom ve moleküldür [2] ve glisinden sonra da olsa hangi atom ve molekülün laboratuvar ortamında daha biyolojik olarak alakalı olduğundan emin değildir. Laboratuvar ortamında, D-serin benzer bağlama potansiyeline sahip gibi görünmektedir [3] [4] [5] fakat sinyal vermede (daha fazla maruz kalma süresi nedeniyle mümkün) 1 μM’de aktiftir. [6]
- NMDA :Sinaptik plastisiteyi ve hafıza fonksiyonunu kontrol etmek için NMDA reseptörü çok önemlidir.
Ayrıca, D-serin eylemi sinaptik NMDA reseptörlerinde lokalize edilmiş gibi görünse de glisin ekstrasinaptik bir etkidaşıdır, [7] ancak doku ölümünü uyandırmak mümkün görünmektedir [8] (bu, geçmişte ekstrasinaptik reseptörlerden dolayı düşünülmektedir N2B altbirimi [9] [10] [11] ve sinaptik daha çok N2A’ya sahip olduğu için). [7]
D-Serin, daha sonra bir sinirden diğerine iletimi düzenleyen sinir sisteminin (glial hücreler) destek hücrelerinden salınan bir sinir düzenleyicisidir. NMDA reseptörlerinin glisin bağlama alanının dahili bir atom ve molekül olduğu görülmektedir.
Diyette yaygın olarak bulunmasa da, diyet Glisinden sentezlenir (bir amino asit)
1.2 Biyolojik Önemi
L-Serin (bir diyet amino asit), göreceli olarak astrositler (beyin ve omurilikte bulunan hücreler) olarak adlandırılan glial hücreler en yüksek serin racemase seviyelerini ifade ederken sinirlerde[12] ve glial hücrelerde [13] bulunan serin racemase enzimi aracılığıyla D-Serin rasemikleştirilir. [14] [15] [16] En çok önbeyinde bulunur; Serin racemase ekspresyonu, D-serin lokasyonu ile iyi ilişkilidir. [14] [15] Serin racemase’den D-serin sentezi oranı, ATP ve Magnezyumun kofaktörlerini (iyonu) gerektirir [17] [18] ve hem kalsiyum [19] tarafından olumlu etkiliyor hem de glisin ve L-aspartik asit tarafından engellenmektedir. [19] [20] [21]
- ATP : Hücre içi biyokimyasal reaksiyonlar için gereken kimyasal enerjiyi taşıyarak vücudun enerji üretmesini sağlar.
- AMPA :Nörotransmitter glutamatın etkilerini taklit ettiği AMPA reseptörü için spesifik bir agonist olan bir bileşiktir.
AMPA reseptörlerinin aktivasyonu, muhtemelen glutamat reseptör etkileşimli proteininin (GRIP) serin racemase ile etkileşime girmesini teşvik ederek etkinleştirildiğinde D-serin konsantrasyonlarında 5 kat artışa neden olur. [22] Son olarak, bu enzim L-serin’i piruvata dönüştüren (D-serin üretimine göre 3: 1 oranlı) ve amonyak olduğu için bu dönüşüm için spesifik değildir. [23]
D-Serin çoğunlukla astrositler (bazıları nöronlarda), L-serinden üretilen serin racemase enzimi ile üretilir.
D-serin, astrositlere özgü d-amino asit oksidaz (DAAO) enzimi tarafından düşürülür. D-Serin konsantrasyonları, DAAO enziminin ekspresyonu / aktivitesi ile ters orantılıdır [4] [27] [24] ve enzimin çıkarılması tüm test edilen beyin bölgelerinde D-serinin yükselmesine neden olur. [24] [25] [26] [28] D-serin, serin racemase enzimi aracılığıyla da L-Serin dönüştürülebilir, ancak bu reaksiyonun tersinden daha az afinitesi vardır. [1]
- DAAO : Amonyak ve hidrojen peroksit üreten ilgili imino asitlere oksitlemek için moleküler seviyede bir fonksiyona sahip bir enzimdir. Bu, çeşitli sistemlerde, özellikle de beyinde, bir dizi fizyolojik etki ile sonuçlanır.
D-serin seviyesini düşüren birincil mekanizma, astrositlerdeki tekrar birikmesidir ve ardından DAAO (ana yol) ya da L-Serin geri dönüşümüdür (küçük yol).
1.3 Diğer Glisinerjikler
Şizofreni semptomlarında azalma derecesine bakıldığında, 30 mg / kg D-Serin [29] ile görülen genel % 17-30 aralığı, benzer şekilde araştırıldığında 800 mg / kg [30] dozunda kullanıldığında glisinden bir miktar mukayese edilebilir. D-serin’in ağırlık bazında daha güçlü olduğunu düşündürmektedir.
Benzer altı haftalık D-serin ve sarkosin (amino asit) dozlarının (2.000 mg) tamamlanması, D-serinin sarkozun plaseboya göre anlamlı derecede daha iyi olmadığı ve sarkozinin daha etkili olduğu sonucuna vardı. [31] Bu, başka yerlerde de belirtilmiştir; aynı miktarda D-serin bulunan sarkozin, semptomların düşmesine neden olur. [32]
D-serin, aynı sinyal verme özelliklerinde ve müdahalelerde glisinden daha güçlü görünse de, sınırlı karşılaştırmalı kanıt, D-serinin, sarkozine (bir glisin taşıma inhibitörü) göre daha düşük performans gösterdiğini ortaya koymaktadır.
2 Farmakoloji
2.1 Kan
30-120 mg / kg’lık (şizofrenik hastalarda), serum D-serin konsantrasyonlarını 1-2 saatlik bir kanda maksimum süresi ile artırdığı bildirilmiştir [33] ve kanda maksimum dozajı değerleri 120.6 ± 34.6 nmol / mL’de bildirilmiştir (30mg / kg), 272.3 ± 62nmol / mL (60mg / kg) ve 530.3 ± 266.8nmol / mL (120mg / kg). [33]
D-Serin takviyesi, oral alımdan 1-2 saat sonra kanda zirve seviyesine ulaşır ve oral alımına 120 mg / kg’a kadar doğrusal doz bağımlılığını izler (en yüksek test edilen doz).
Parkinson hastalığı olan kişilerde altı haftalık D-Serin (30 mg / kg) takviyesinin, serum D-serin düzeyini 10μM’den 120.0 ± 52.4μM’ye düşürdüğü ve PTSD’li kişilere benzer şekilde büyük bir artış sağladığı kaydedildi [ 10 misli), aynı oral dozda görüldü ve serum konsantrasyonları 146 +/- 126.26uM’ye ulaştı. [35]
- PTSD : Doğal afet, ciddi kaza, terörist olay, sevilen birinin ani ölümü, savaş, tecavüz gibi şiddetli kişisel saldırı veya diğer yaşamı tehdit eden olaylar yaşamış veya şahit olmuş kişilerde meydana gelebilecek potansiyel olarak zayıflatıcı bir durumdur. .
Şizofrenide, aynı dozun 102.0 +/- 30.6nmol / mL’den 226.8 +/- 72.8nmol / mL’ye (% 122 artış) [29] yükseldiği ve istirahatte ortalama serum seviyelerinin 30-120mg arasında 4 hafta boyunca oral D-serin alımı ile doza bağımlı bir şekilde arttığı gözlenmiştir. 4 haftada oral D vitamini alımı. [33]
D-serinin bazal seviyeleri, bazı çalışmalarda yaklaşık 10 kat artışa neden olmakla birlikte şizofrenlerde daha düşük (ve halen mevcut) bir artışa neden olan 30 mg / kg D-serin takviyesinin ardından artmaktadır.
Supplement D-serin, kan glisin, glutamat veya alanin konsantrasyonlarını etkilemez [29] [35] ve kan L-serin de etkilenmez gibi görünmektedir. [35]
Serum metabolizması ile ilişkili olabilen serumda D-Serinin önemli ölçüde diğer amino asitleri etkilediği gözükmemektedir.
2.2 Sinirsel
Beyindeki D-serin konsantrasyonları, toplam serin havuzunun % 10-15’i arasında bir yerde olan 66 ± 41nmol / g yaş ağırlık [36] veya 2.18 ± 0.12nmol / mg [37] arasında görünmektedir ( L-serin ile sayıları daha fazladır). [36] [37] D-serin, serebellum ve omuriliklere kıyasla prefrontal ve parietal kortekste daha yüksek konsantrasyonlarda bulunur. [38] D-serin, beyinde 16 saat yarılanma ömrüne sahiptir [39] ve beyindeki D-serin konsantrasyonundaki artışlar, 58 mg / kg (fareler) kadar düşük dozlarda görülmektedir. [40]
D-serin kontrol kişilerin beyin omurilik sıvısında (2.72 ± 0.32 uM) [41] [42] tespit edilmiştir ve postherpetik nevraljisi (kronik bir ağrı sendromudu) olan kişilerde (1.85 ± 0.21μM) ve dejeneratif kireçlenme (3.97 ± 0.44 μM) [41] şizofrenide D-serin konsantrasyonları kontrol grubuna göre daha düşüktür (ortalama değer 1.43 μM’e karşı 1.26 μM’ye, aralıklar önemli ölçüde farklı değildir). L-serin yüksek (22.8 +/- 8.01μM’ye karşılık 18.2 ± 4.78μM) ve L-serin ile D-serin arasındaki orandır. [42]
D-Serin, beyin omurilik sıvısında (CSF) ve beyinde bulunur, burada CSF’de kandan daha düşük konsantrasyonlarda bulunur ve beyinde kandan daha uzun bir yarılanma ömrüne sahiptir.
D-Serinin kronik kullanımı, farelerin korteksindeki L-serin düzeylerini artırabilir. [40]
3 Nöroloji
3.1 Düzenleme ve Dağıtım
D-serinin, glutamat salgıladığı bilinen uyaranlar kullanılırken D-serine, glutamatta glutamatla birlikte sinirlerde ve astrositlerde (beyin ve omurilikte bulunan hücreler) depolandığı düşünülmekte ve D-serinin bir glutamat taşıyıcısını ifade eden nöronlarda saptanmaktadır. [44]Bu gözlenme ve serbest bırakma, glutamat ve glisin ile başka yerlerde kaydedildi.
D-Serin, iki ayrı bölgenin (bir tanesinde glisin veya serin gerektirir) aktivasyonunun birlikte yapılması gerektiğinden sinirlerde glutamat ile birlikte NDMA reseptörlerini aktive etmek mümkündür. Sinirsel salım, D-serinin sinaps için bir kısmını, ancak çoğunluğu sağlamaz.
D-Serin glio-transmitter, glial hücrelerden salınan sinir düzenleyici bir madde olarak bilinir. [45] [14] [46] D-serinin bazı veziküler molekül çıkarımı yoluyla serbest bırakıldığı düşünülmektedir [47] (bu veziküler glia’da tespit edildiği için [48] [43] ). Sinaptik veziküllerin, glisin, glutamat ve GABA (ancak D-serin değil) birlikte eksprese ettiği bulunmuştur. [49] [50] [51] D-serinin kendine özgü veziküler depolaması olduğu düşünülmektedir. [52] [49] [47] Asc-1 ve TRPA1 taşıyıcıları dahil edildiği için veziküller D-serin salınımının tek yöntem olmayabilir (sırasıyla doğrudan nakil ve destekleyici kalsiyum akını) ve veziküler depolamayı bastırmak D-serin salımını ortadan kaldırmaz. [50] [53]
- TRPA1 :Birçok insan ve hayvan hücresinin plazma membranı üzerinde bulunan bir iyon kanaldır. Bu iyon kanalı en çok ağrı, soğuk ve kaşıntı gibi somatosensoriyel modalitelere yol açan çevresel irritanlar için bir sensör olarak bilinir.
D-serin’in astrosit salımı, NDMA’ya bağlı işlemler için hayati önem taşımaktadır (hipokampal kültürlerden astrositlerin alınması, uzun süreli potensiyasyonu baskılamaktadır ve bu D-serin ile restore edilmektedir). [54]
D-Serinin astrositlerden salınması (gliyal hücreler) beyindeki D-serin salınımının baskın şekli olarak görülür (nöronal salım daha küçük bir toplam miktardır) ve serbest bırakmaya aracılık eden mekanizmalar bu noktada zamanında bilinmemektedir. Ancak glutaminerjik sinyallemede hayati önemi olduğu bilinmektedir.
Nitrik oksitin (NO) serin racemase aktivitesini baskılayabileceğini [55] ve DAAO aktivitesini arttırdığını ve dolayısıyla D-serin konsantrasyonlarını negatif olarak düzenlediğini (D-serin bir Nitrik oksit sentezi olduğu için karşılıklı olabilir (NOS) ). [55] NMDA reseptörlerinin aktivasyonu, NOS aktivasyonuna neden olduğundan ve Nitrik oksit konsantrasyonlarını arttırdığından potansiyel olarak negatif bir geribildirim döngüsüdür. [1] [57]
- NOS : L-arginin’den nitrik oksit üretimini katalize eden bir enzim ailesidir.
Glutaminerjik sinyal kaynaklı nitrik oksit metabolizmasının harekete geçirilmesi D-serin üretimini olumsuz şekilde düzenler ve böylece D-serinden sinyal gelişimini sınırlandırabilir.
D-serin’in (50 mg / kg) farelere organlara enjeksiyonu, bellekte düzelme ile ilişki gösteren, 96.9 nmol / g’dan 159.4 nmol / g’ye (% 64.5 artış) kadar hipokampal D-serin konsantrasyonlarını artırdığı kaydedildi. [58] Bu değişiklikler, glutamat veya L-serin konsantrasyonları üzerinde herhangi bir etkiye sahip değildir. [58]
Vücudun dolaşımda D-Serinin hipokampal D-Serin konsantrasyonlarını arttırdığı bilinmektedir, bu da kan beyin bariyerini geçtiğini düşündürmektedir.
Glisin büyük ihtimalle omurilikte ve arka bölgede NMDA reseptörlerinin glisin bağlanma bölgesinin ana etkidaşıyken, ön beyin muhtemelen daha yüksek serin racemase ekspresyonundan ötürü D-serin tarafından etkilenmiştir (ve dolayısıyla daha fazla D- serin sentezi) [4] [14] [45] [22] ve glisin astrositlerin içine alan glisin taşıyıcılarının daha yüksek ekspresyonudur. [59] [60] D-Serin, NMDA reseptörlerinin nerede ifade edildiği ile ilişkili olarak ön beyin alanında [61] daha yüksek olduğu doğrudan ölçülmüştür. [4] [45] [62]
D-Serin muhtemelen, ön beyin bölgelerinde glisin’den daha biyolojik olarak alakalıdır.
3.2 Glutaminerjik Sinyalizasyon
D-Serin, NMDA reseptörleri (NR2’nin [63] [64] alt tipi, NR2 olarak glutamatı bağlar ve herhangi bir NMDA reseptörü, genellikle her ikisinden oluşan bir tetramerdir) üzerinde glisin bağımlı bağlanma bölgesine bağlanabileceği ve daha sonra başlangıçta glutamat veya diğer etkidaşların neden olduğu bu NMDA reseptörleri aracılığıyla sinyalleşmeyi güçlendirebilecek şekilde Glisine benzer birçok mekanizmayı paylaşır. [63] [6] [6] 66]
- NR 1/ 2 : Alzheimer hastalığında glutamat reseptörünün alt tipleridir.
Glisin’den farklı olarak, D-Serin daha etkili gibi görünmektedir ve 1μM kadar düşük bir konsantrasyonda (10μM’yi gerektiren Glisin) [6] aktiftir ve bu da reseptörün kendisi üzerinde oynama ile ilgili olmayabilir (ikisi oldukça karşılaştırılabilir). [3] [4] [5] Ancak glisin ile olduğundan daha az glial hücrenin serine geri alımından kaynaklanıyor olabilir. [67]
D-serin’in sinaptik konsantrasyonlarındaki herhangi bir artışa, glisin’e (veya glisin bağlanma bölgesini aktive edebilecek herhangi bir şey) benzer şekilde NMDAergic sinyalizasyonunda bir artış da eşlik eder [59] [68] [69] , aktiviteye bağlı olduğu düşünülmektedir; glisin bağlama sahasında hız sınırlayıcıdır. Hipokampus, talamus, neokorteks, beyin sapı ve retinanın bulunduğu birçok beyin bölgesinin glisin bağlanma sahasının doymamış olduğu ve bu nedenle ek glisin veya D-Serine yanıt verdiği kaydedildi. [6] [70] [59] [71] [72]
D-Serin, Glisin’e benzer şekilde, NMDA reseptörünün glisin bağlama yerindeki bir atom ve moleküldür ve bu NMDA reseptörleri vasıtasıyla glutaminerjik sinyal vermeyi güçlendirme kabiliyetine sahiptir. Reseptör seviyesinde aynı derecede güçlüdürler, ancak D-Serin daha biyolojik olarak alakalı görünür ve genel olarak da güçlüdür.
D-Serinin, 3.7 ± 0.1 mM’lik bir IC50 ile AMPA reseptörleri üzerinde (kainat asidi tarafından uyarılan) konsantrasyona bağlı bir engelleyici etkisi olduğu görülmektedir. [73] L-Serin’in bu etkisi yoktur, [73] ancak bu konsantrasyon alakalı olamayacak kadar yüksek olabilir.
- IC50 : Bir maddenin belirli bir biyolojik veya biyokimyasal işlevi bastırma gücünün bir ölçüsüdür.
- AMPA : Nörotransmitter glutamatın etkilerini taklit ettiği AMPA reseptörü için spesifik bir agonist olan bir bileşiktir.
AMPA reseptörleri üzerinde önleyici etkiler olmasına rağmen, konsantrasyon çok yüksek gibi görünmektedir ve pratik olarak uygun olmayabilir.
Doku ölümü açısından D-serin ve glisin, NMDA reseptörleri üzerindeki glisin bağlanma yerlerini etkinleştirmek için gereken dozlardan 50-100 kat daha fazla konsantrasyonda olan 47 uM ve 27 uM (sırasıyla) ED50 (etkili doz) değerleri ile glutamat kaynaklı doku ölümünü güçlendirmektedir. [74]
Doku ölümünün arttırılması NMDA reseptörleri değil, glisinerjik reseptörlerin aktivasyonu ile sağlanır. GABA (GABA A reseptörleri vasıtasıyla etki ederek), NMDA kaynaklı doku ölümünü de güçlendirebildiğinden, sinirde klorür akışı olduğuna karar verilmiştir. [74]
Glisinerjik reseptörler aracılığıyla aşırı sinyal iletimi, NDMA’nın neden olduğu yan etkileri güçlendirirken, bunun meydana geldiği konsantrasyonlar NMDA reseptörlerini aktive etmek için gerekli olanlardan daha yüksek görünmektedir. Bu verilerin pratik önemi bilinmiyor.
3.3 Glisinerjik Sinyal
Glisinerjik sinyal (bastırıcı ve glisin reseptörleri vasıtasıyla [75] ve nöronlara klorin akışı oluşturur), D-serin takviyesi ile de ortaya çıkabilir. İki amino asit arasındaki glisinerjik sinyalleri karşılaştıran çalışmalarda, düşük EC50 değerleri (27μM v. 47μM ile kanıtlandığı gibi) glisin daha güçlü olma eğilimindedir. [74]
Glisin geri alımına aracılık eden taşıyıcılar (Glisin taşıyıcı-1 ve 2) [76] [77] ve daha genel olarak alanin-serin-sistein taşıyıcı-1 (AscT1) hem glisin hem de serine aracılık edebilir (her iki bileşeni). Bu nedenle D-serin ve glisin, sarkozinden etkilenir. [78] [79]
D-Serin, ayrıca, glisinerjik reseptörler üzerinde sinyal özellikleri paylaşır ve glisin’in aynı taşıyıcılara tabi tutulur.
3.4 Oksidasyon
D-Serin, aşırı uyarılma ve ortaya çıkan kalsiyum akışı oksidatif hasara neden olan aşırı-uyarılma NMDA reseptörlerine ikincil oksidasyonu uyarmak için deneysel olarak kullanılabilir. [80] D-serin kaynaklı aşırı-uyarılmadan kaynaklanan bu oksidatif hasar laboratuvar ortamında [81] ve COX2 inhibitörleri ile zayıflatılmış bir mekanizma ile 50-200mg / kg (fareler) [82] [83] laboratuvar ortamında bastırılmıştır. [81]
- COX2 : Artrit rahatsızlıklarının, adet kramplarının ve spor yaralanmaları gibi akut yaralanmaların acılarını tedavi etmek için kullanılan reçeteli ilaçlardır.
COX2, iskemi, travmatik beyin hasarı [86] ve Alzheimer [87] gibi NMDA aşırı-uyarımına neden olan stres faktörlerinin ardından aşırı eksprese olma eğilimindedir. Bu uyarma reaktif oksijen türlerinin üretimine aracılık ettiği için, COX2 inhibitörlerinin NDMA toksisitesine karşı sinir koruyucu olabilir. [88]
- NDMA : Beyinde ve omurga kolonundaki nöronlar arasındaki elektrik sinyallerinin transferine izin veren bir iyonotropik reseptördür.
Bu mekanizmaların, Alzheimer gibi bazı patolojik koşullarla ilişkili olduğu düşünülse de, supplement D-serin ile oksidatif hasarın etkileşimleri belirsizdir.
Aşırı dozlar veya aşırı doz D-serin oksidatif hasara (NMDA sinyalini çok arttırarak yan etkiler oluşturur) neden olabilir ve aşırı kimyasal D-serin metabolizmasının bazı hastalık durumlarında da rol oynadığı düşünülmektedir.
Besin takviyesi etkisi belirlenmemiştir, ancak oksidatif hasar standart supplement dozajların çok üzerinde olmayan dozlarda uyarıldı.
3.5 Hafıza ve Öğrenme
Glutaminerjik sinyalizasyonun bellek oluşumunu arttırdığı bilinmektedir; çünkü NMDA reseptörlerinin aktivasyonu, hafızanın mekanik temelini oluşturan uzun vadeli potentiasyon (LTP) sağlamak için çalışan kalmodulin bağımlı kinaz (CaMK) ve CREB bağlama proteininin kalsiyum akışı ve mobilizasyonuna neden olur. [89] [90] Magnezyum L-Threonate ile birlikte görülen hafıza arttırıcı mekanizmasıdır ve NMDA sinyallemesinde artışa neden olan (özellikle NR2B alt birimi aracılığıyla) bellek ve LTP artışına neden olur. [91] [92]
- LTP : Nörobilimde, son aktivitelerine dayanan sinapsların kalıcı olarak güçlendirilmesidir. Bunlar, iki nöron arasındaki sinyal iletiminde uzun süreli bir artış sağlayan sinaptik aktivite modelleridir.
- CaMK : İştahı uyaran hormon nöropeptid Y üretimini düzenler ve hipotalamusta bir AMPK kinaz olarak işlev görür.
- CREB : Hücresel bir transkripsiyon faktörüdür. CAMP yanıt elementleri (CRE) olarak adlandırılan belirli DNA dizilerine bağlanır, böylece genlerin dna’dan rna’ya dönüşümü artar veya azalır.
D-serin, NMDA reseptörü (1μM’de % 52 ± 16 arttırma ve 30μM’e kadar artan aktivite) ile sinyallemeyi arttırma kabiliyeti nedeniyle [6] bu süreçte D-serin canlılığı ile eşleştirilmiştir. [54] Hipokampal hücrelerin D-Serin uyarımına duyarlılığı bilinmektedir, [70] supplement D-serin’in bellek ve öğrenmeyi teşvik edebileceği düşünülmektedir. [58]
Sinaptik plastisiteye aracılık eden ve LTP’yi dolaylı olarak etkileyebilen uzun vadeli depresyon (LTD; LTP’nin zıttı değil) olarak bilinen ve D-serin 600-1000 mg / kg enjeksiyonlarda [95] aktive olabilen başka bir olay vardır. [95] [96] Laboratuvar ortamında çalışmalarla, 5μM’de (%2 3μM ve 10μM konsantrasyonlardan daha etkili olan, kontrolünde % 19.3’ten % 58.3’e kadar) LTD büyümesinde etkili olduğunu belirtti. [96] Görünüşe göre, D-Serin ait LTD, glutaminerjik etkileri yoluyla aracılık edilmektedir [96] ve LTD boyunca daha fazla D-serin, astrositlerden salınmaktadır. [96]
- Sinaptik plastisite : Sinirbilimde sinaptik plastisite, sinapsların aktivitelerindeki artış veya azalmaya yanıt olarak zaman içinde güçlendirme veya zayıflama yeteneğidir.
D-Serin hafıza oluşumunu hızlandırmada rol oynayabilir ve NMDA reseptörleri vasıtasıyla glutaminerjik sinir iletiminin arttırılmasına ikincildirler (D-serin glisin bağlama bölgesini aktive edebilir).
Yaşlanma ile ilgili süreç, en azından hipokampusta olduğu gibi, subaktif glutaminerjik reseptör sinyali ile ilişkili gibi görünen kalsiyuma bağımlı nöronal plastisiteyi [97] [98] sürmek için azalmış bir yeteneğe bağlıdır (özellikle NMDA). [99] 100] Yaşlanma sürecinde beyindeki azalan D-serin konsantrasyonları nedeniyle [101] (muhtemelen serin rasemase ekspresyonunun azalmasıyla ilişkili) [102] ve önceki teorinin başarısızlığı (NMDA reseptör ekspresyonunda yaşa bağlı düşüş [103] [104] azalmış NMDA reseptör ekspresyonu, bilişsel azalmaya neden olmadığı için ilgili olmayabilir [105]) artık NMDA reseptörünün glisinergik bağlama bölgesinde azalmış aktivitenin yaşa bağlı düşüşe katkıda bulunduğu düşünülmektedir ( NMDA sinyalizasyonu ve dolayısıyla sinaptik plastisite vasıtasıyla).
Ayrıca, yaşla ilişkili bilişsel bozukluğun D-serin ile korunduğunu ve NMDA’ya bağlı plastisitenin D-Serin bağımlı olduğunu kaydeden çalışmalarla desteklenmektedir. [13] [106] [107] [108]
Yaşlanma süreci D-serin üretiminde bir azalmaya neden olur (nedeni tam olarak bilinmemektedir) ve düşük D-serin seviyeleri NMDA sinyalini azaltır ve bu nedenle yaşa bağlı bilişsel düşüşe katkıda bulunabilir.
Müdahalelerle ilgili olarak, 50 mg / kg D-serin verilen normal olmayan farelerde yapılmış bir çalışma, D-serin’in tek bir doz sonrasında ve çoklu dozlardan sonra hafıza oluşumunu iyileştirmeyi başardığını belirtti. [58] 50 mg / kg D-Serin’in potensi, bilişsel güçlendirici olarak bilinen 20 mg / kg D-Sikloserine [58] karşılaştırılabilir gibi görünüyor. [109] [110]
D-serin, eğitimden 30 dakika sonra verildiğinde etkili olur ve bellek konsolidasyonunda yardımcı olduğunu düşündürür. 6 saat sonra verildiğinde etkisizdi. [58]
MK-801’in oluşturduğu hafıza kaybının bozulması D-serin ile zayıflamış gibi gözükmektedir. [58]
- MK-801 : MK-801 olarak da bilinen Dizosilpine, 1982 yılında Merck’te bir ekip tarafından keşfedilen bir glutamat reseptörü olan N-Metil-D-aspartat reseptörünün, bilişsel olmayan bir antagonistidir.
D-Serin takviyesinin sağlıklı kemirgenlerdeki hafıza oluşumunu artırabileceği mümkündür ancak çalışmalar halen enjeksiyonları kullanan ve bazıları oldukça büyük dozaj alan kişilerdir (50mg / kg insan eşdeğeri 3mg / kg olmasına ve oldukça mantıklı olmasına rağmen).
Kısa süreli olarak (bilişsel testlerden iki saat önce) sağlıklı erişkin bireylerde 2.1 g D-serin kullanan bir çalışma sürekli dikkat ve anında kelime hatırlamada iyileşme için sürekli performans testinde (CPT-IP) gelişmiş performans buldu; basamaklı ilerleme görevinde bir gelişme oldu, geriye doğru saymada değil. [111]
- CPT-IP : Dikkat sorunlarını ve tedaviye yararlılığını değerlendirir.
Bilişte, sağlıklı yetişkinlere D-serin takviyesi verildiğinde küçük ilerlemeler olabilir.
3.6 Depresyon
D-serin sentezinin veya farelere kronik takviyenin genetik aşırı ekspresyonu (beş haftada 58 mg / kg), başlangıçta normal olmayan farelerde anti-depresan etkilere neden olur gibi görünüyor. [40]
D-serin takviyesinin bazı küçük anti-depresif etkileri olabilir ve bunlar daha fazla incelenmelidir.
3.7 Alzheimer ve Bunama
NMDA aracılı sinir-iletimi Alzheimer hastalığında rahatsız edici görünmektedir ve bellekte [112] [113] ve sinaptik oluşumda [114] düşüşe bağlı olarak davranışsal açıklarla sonuçlandığı düşünülmektedir. [115] Şizofreni hastalarının aksine, Alzheimer’teki sinyal, beta-amiloid peptidlerin (β-amiloid), sinapsda hem glutamat hem de D-serin biriktirebildiği ve her ikisinin de serbest bırakılmasını teşvik ettiği [116] [117] [117] [118] bunların hepsi yan etkisine katkıda bulunabilir (aşırı glutaminerjik sinyalleme hücresel hasara neden olur).
- Beta-amiloid : Alzheimer hastalarının beyinlerinde bulunan amiloid plakların ana bileşeni olarak Alzheimer hastalığında çok önemli rol oynayan 36-43 amino asitten oluşan peptidleri ifade eder.
Alzheimer hastalarının kontrolüne göre D-serin konsantrasyonlarında belirgin tedirginlik gözükmemektedir. [36]
D-serin, beta-amiloid pigmentasyona bağlı olarak Alzheimer hastalığının patolojisinde rol oynayabilir.
3.8 Şizofreni
Şizofreninin semptomlarının (özellikle olumsuz belirtiler) glutaminerjik hipofonksiyon ile ilişkili olduğu düşünülmektedir ve glutaminerjik ateşlemeyi (glutamat reseptörleri yoluyla azaltılmış toplam sinyalleme kapasitesi) yeniden tesis etmeyi amaçlayan son farmakolojik tedaviler arasında serin / glisin restorasyonu (toplam yüksek serine ve glisin şizofrenlerde kontrole kıyasla daha yüksek olmasına rağmen [121] [122] D-serin’in kendisi [123] azalmış ve serin rasemaz ile ilgili problemler düşündürmektedir [124] [125]) yer alır; çünkü, NMDA reseptörlerine glisin bağlanmasını bozan şizofreni ve serin rasemase geni değiştirilmiş farelerinin (veya D-serinin üretimini azaltmak için herhangi bir şey) şizofrenik semptomları da vardır [ 127] [128] ancak D-amino asit oksidazın çıkarılması (ve D-serin’in bozulmasını önleyerek) rehabilite edicidir. [129]
Son olarak, şizofreninin klinik hafiflemesinde , D-serin konsantrasyonlarında takviyeden bağımsız olarak bir artış eşlik eder. [130]
Diğer muhtemel tedavi edici seçenekler arasında, AMPA reseptörleri (bu Piracetam ve Aniracetam’ı içerir) aracılığıyla sinyallemeyi arttıran AMPAkine’leri içerir [131] ve dolaylı olarak, glisin alımlarını hücrelere engelleyerek ve sinaptik etkilerini (sarkozin [132] ile birlikte görerek) destekleyerek yukarıda belirtilen NMDA sinyalini desteklemektedir. AMPA sinyallemesinin güçlendirilmesi doğal olarak glutaminerjik sinyali artırır ve NMDA reseptörlerinden magnezyum bloğu kaldırabilir. [133] [134]
Şizofreninin negatif semptomları, duygusal sığlaşma ve sosyal izolasyona atıfta bulunurken halüsinasyonlar, sanrılar ve düşünce bozukluğu, ‘pozitif’ semptomlar ilişkili kognitif bozukluklar olarak adlandırılmamaktadır. [135] [136]
D-Serin uygulaması, NMDA glisin bağlanma yerini etkilemek suretiyle ve dolayısıyla NDMA reseptörleri vasıtasıyla sinyal vermeyi pozitif olarak düzenleyerek, şizofreni semptomlarını azaltabildiği düşünülmektedir. Bu durum şizofreninin bir D-serin eksiklik durumu gibi gözükmesiyle desteklenmektedir (sebep ya da etkide rol oynamamaktadır).
Pozitif ve Negatif Sendrom Ölçeği (PNSS) tarafından değerlendirilen sınırlı pozitif çalışmalar, şizofreni negatif belirtilerinde 30 mg / kg (toplamda 2.12 ± 0.6g genel) D-serin ile % 17-30’luk bir iyileşme olduğunu belirtmektedir (Benzer araştırma koşullarında 800mg / kg Glisin ile benzer potens). [29] [30] Olumsuz belirtilerin ilerlemesini ölçen çalışmalarda, takviyenin 2 hafta içinde faydalı etkilere dikkat çekilir; bu, gözlemin gücünü 6 hafta boyunca arttırır ve 60-120mg / kg aralığında daha yüksek dozlarda daha belirgindir. [29] [137] [33]
Spesifik olarak pozitif belirtilere bakıldığında, 30 mg / kg (toplamda 2.12 ± 0.6g) D-serin 6 haftadan sonra belirgin düzelme gösterdi ancak, 2. ve 4. haftalarda kaydedilen eğilim istatistiksel olarak anlamlı değildi. [29] 60-120mg / kg ile 30mg / kg’dan daha yüksek oranlarda düzelmeler kaydedildi ve hem pozitif hem de negatif semptomlardaki faydalar D-Serin serum maruziyeti ile ilişki gösterdi. [33]
Standart anti-psikotik ilaçlara ek olarak, şizofreni tedavisinde 16 haftalık 2.000 mg D-serin, şizofreni tedavisinde 16 haftalık günlük plaseboya göre takviye önemli bir yarar bulamadı, ancak yazarlar normal plasebodan daha büyük yanıtın kısmen sonuçlarını açıklayabileceğini bildirdi. [138 ]
Buna rağmen D-serin 30 mg / kg veya 2.000 mg’lık dozajda herhangi bir yerde plasebodan anlamlı olarak farklı bulunmamıştır. [31] [32] [139] Bu çalışmalar, bireylerin istatistiksel önemi elde etmek için yeterli olmamakla birlikte yarar elde ettiklerini ve bunun, kandaki D-serin ile semptomların faydaları arasındaki ilişkiyle eşleştirildiğini belirtmektedir. [33] Oral terapiden serum D-serinde saptanan çeşitlilik, gözlemlenen zayıf etkilerin altında yatabilir.
D-Serin, şizofreninin tüm semptomlarını azaltmada (çoğunlukla olumsuz ve bilişsel, pozitif etki de daha az olmakla birlikte) etkili gözükmektedir ancak 30 mg / kg standart önerilen doz güvenilmez gibi görünmektedir. Bu, D-serin’in kana ne kadar ulaştığının büyük bir değişkenliğine bağlı olabilir ve daha yüksek dozlar almak kısıtlı kanıtlara dayalı olarak daha güvenilir görünmektedir.
3.9 Parkinson Hastalığı
Parkinson hastalığının şizofrenideki negatif belirtilere (ilgisizlik , düz etki ve izolasyon) benzer bazı belirtileri (motivasyon, sürüş ve başlangıç / duygusal tepki [140] [141] bozuklukları) var gibi görünüyor ve benzerliklerinden dolayı D-serinin faydalı olabileceği düşünülmektedir. [34] Ayrıca, striatumdaki dopaminerjik nöronlar NMDA sinyalizasyonunda yer alırken, [142] Parkinson hastalarında NMDA reseptörlerinin değiştiği bilinmektedir. [143]
Parkinson hastalığına sahip 13 kişiyle (günlük 1,600-2,600 mg aralıklarla sonuçlanan) küçük bir pilot çalışmada altı haftalık 30 mg / kg D-serin ilavesi, Birleşik Parkinson Hastalık Değerlendirmesi ile değerlendirilen semptomları azaltmayı başardı; Ölçek, Simpson-Angus ölçeği ve Pozitif ve Negatif Sendrom Ölçeğiydi. [34] Bu çalışmada semptomlarda % 20 iyileşme gösteren deneklere bakıldığında, D-serin grubundaki kişilerin % 50-70’inin bu ölçütleri karşıladığı, buna karşılık % 10-20’lik bir oranla plasebo da uygulandığını belirtti. [34]
Ön kanıtlar D-serinin Parkinson hastalığının tedavisinde yararlı olabileceğini öne sürdü.
3.10 Stres ve Travma
NMDA reseptörleri, çözüşümlü ve algılamalı değişiklikler de dahil olmak üzere PTSD’nin bazı semptomlarında bir miktar rol oynamaktadır [144] ve ketamine (NMDA karşıtı) de bu belirtilere neden olabilir. [145] Çünkü NMDA’nın çok düşük ateşlemesiyle, özellikle de hipokampusta veya amigdalada kaynaklandığı düşünülmektedir. [35]
- PTSD : Doğal afet, ciddi kaza, terörist olay, sevilen birinin ani ölümü, savaş, tecavüz gibi şiddetli kişisel saldırı veya diğer yaşamı tehdit eden olaylar yaşamış veya şahit olmuş kişilerde meydana gelebilecek potansiyel olarak zayıflatıcı bir durumdur. .
D-Sikloserin (NMDA reseptörlerinin glisin bağlanma yerinde kısmi etkidaşı, buna karşın D-serin tam bir etkidaşıdır), travma sonrası stres bozukluğunun semptomlarını azaltmak için bir pilot çalışmada daha önce yarar sağlamıştır (TSSB, uyuşma, kaçınma ve kaygı semptomlar çoğunlukla). [146] Altı haftalık 30 mg / kg’da D-serin kullanan bir çalışmanın anksiyete belirtilerinde (HAMA; % 13.4 % 46 CI, % 13.4-46.7 semptom azalması), depresif (HAMD; % 95 GA % 2.0-43.3 semptom azalması) ve CAPS skoru (% 95 GA, % 10.9-31 azalma). [35]
Ön kanıtlar, Post Travmatik Stres Bozukluğu’nun semptomlarının tedavisinde fayda sağladığını göstermektedir, ancak gözlemlenen faydalar oldukça güvenilmez görünmektedir.
3.11 Amyotrofik Lateral Skleroz
Farelerde amyotrofik lateral skleroz (ALS), ALS’ye duyarlı nöronların NMDA aracılı eksitotoksik hasara ne kadar sahip olduğunu tahmin edebilen spinal sıvının D-serin konsantrasyonlarında % 50-100 yükselme ile ilişkilidir. [147] [148] [147] Bu, artmış D-serinin ALS patolojisine katkıda bulunduğunu ileri sürmesine rağmen, serin razemase enzimini engellemenin hastalık başlangıcını hızlandırdığını (paradoksal olarak tanımladı), ancak hastalığın ilerlemesini yavaşlattığını; bunun da D-serin takviyesiyle taklit edildiği belirtilmektedir. [148] [149]
- ALS : Esas olarak, kas hareketini kontrol etmekle sorumlu sinir hücrelerini (nöronları) içeren bir grup nadir nörolojik hastalıktır.
D-Serinin, ALS patolojisi ve başlangıcı üzerinde belirsiz etkileri vardır.
3.12 Bağımlılık
Kokain bağımlılığının NMDA reseptörlerine (hem uzun dönem potansiyasyon (LTP) hem de uzun vadeli depresyon (LTD) ilgili olduğu düşünülmektedir) bağımlılık davranışından önce gelen glutamaterjik sinaptik plastisite değişikliklerine neden olduğu bilinmektedir. [150] [151] [152] [153] [154]
D-Serin’in, NMDA hipoaktivitesine katkıda bulunduğu düşünülen kokain çekilme işlemine maruz kalan farelerin nükleus accumbens çekirdeğinde azaldığı ve D-serine sahip nöronal dilimlerle kuluçka olduğu düşünülen, LTP ve LTD’de kokainin neden olduğu değişiklikleri normalize ettiği bildirilmiştir. [155] Bu, kokain bağımlı farelere 10-100 mg / kg D-serin oral yoldan (veya 100 mg / kg enjeksiyon) ilaç arama davranışlarını azalttığı zaman doğrulandı. [156] [157] [158]
D-serinin sukroz tercihini nasıl etkilediğini değerlendiren çalışma, supplementin önemli bir faydasını bulamadı. [156]
Kokain bağımlılığı, NMDA işlevindeki değişikliklerden dolayı sinaptik plastisitedeki değişikliklerle ilişkilidir ve D-serin, kokain geri çekilmesi uygulanan sıçanlarda azalmış olarak görülmüştür. Ön kanıtlar, D-serinin anti-bağımlılık özelliklerine sahip olduğunu ileri sürmektedir.
4 Güvenlik ve Yan Etkileri
4.1 Genel
Altı haftaya kadar olan periyotlar için günde 30 mg / kg D-serin (yaklaşık 2.000 mg) kullanmaya meyilli insan çalışmaları, herhangi bir yan etkiye rastlanmamıştır [138] [29] [33] [35] [34 ] ] 120 mg / kg (yaklaşık 8.000 mg) kullanan bir ön çalışma ile kontrol ile karşılaştırıldığında önemli yan etkiler bulamadı. [33]
D-serinin standart supplement dozajları, standart dozaj aralığında tedavi ile ilgili önemli yan etkileri not etmemektedir.
Moleküler Formül: C3H7NO3
Moleküler Ağırlık: 105.093 g / mol
(D-Serin için yaygın yazım hataları arasında Serine, serin, D-Serin bulunur)
Bilimsel Destek ve Referans Metni
D-Serin Referanslar
- Beyinde D-serin sinyal: arkadaş ve düşman .
- N-metil D-aspartat reseptörü glisin bölgesi ve D-serin metabolizması: evrimsel bir bakış açısı .
- N-metil-D-aspartat reseptör kompleksinin modülatör bölgesi olarak bir {3H} glisin tanıma bölgesinin karakterizasyonu .
- D-serin, endojen bir sinaptik modülatör: astrositlere lokalizasyon ve glutamat ile uyarılmış salınım .
- D-sikloserin, Xenopus oositlerinde ifade edilen NMDA reseptörünün glisin modülatör alanında kısmi bir agonist olarak görev yapar .
- Glycine alımı, eksitatör sinapsların NMDA reseptörlerinde glisin yer işgalini yönetir .
- Sinaptik ve ekstrasinaptik NMDA reseptörleri farklı endojen koagnistler tarafından kaplıdır .
- D-serin: fizyoloji ve patoloji .
- Kültürlenmiş hipokampal nöronlarda sinaptik ve ekstrasinaptik NMDA reseptörü NR2 alt birimleri .
- NMDA reseptör yüzey hareketliliği NR2A-2B alt birimlerine bağlıdır .
- GluN2 C-terminal alanının alt tipi, eksitotoksik hakaretlere olan cevabı belirler .
- Sıçan beyindeki bazı nöronlarda D-serin lokalizasyonu ve üretimi için immünhistokimyasal kanıtlar .
- Astrositlerin D-serin salınımı yoluyla hipokampal uzun süreli potansiyele katkısı .
- Serin rasemaz: glutamat-N-metil-D-aspartat nörotransmisyonunu düzenlemek için D-serin sentezleyen bir glial enzim .
- İnsan serin bir rasemazın karakterizasyonu ve lokalizasyonu .
- Memeli beynindeki D-serin dağılımının immünositokimyasal analizi, glia ve nöronlarda yeni anatomik bölümlendirmeleri ortaya çıkarır .
- Serin rasemazın kofaktörleri, N-metil-D-aspartat (NMDA) reseptör koagneri D-serin’in sentezini fizyolojik olarak uyarır .
- Fare beyin serin rasemazının allosterik regülasyonu .
- Direkt kalsiyum bağlanması, beyin serin rasemaz aktivasyonu ile sonuçlanır .
- Fare serin rasemazında çift substrat ve reaksiyon spesifitesi: yüksek afiniteli dikarboksilat substrat ve inhibitörlerinin belirlenmesi ve beta-eliminaz aktivitesinin analizi .
- Serin rasemaz aktivitesinin amino asitlerle düzenlenmesi .
- Serin rasemaz: glutamat reseptörü ile etkileşime giren protein ve nöronal migrasyonun aracılık yoluyla glutamat nörotransmisyonu ile aktivasyon .
- Fare beyin serin rasemazı L-serin’in pirüvata spesifik eliminasyonunu katalize eder .
- Kültürlenmiş sıçan astrositlerinde D-amino asit oksidazın gen ekspresyonu: bölgesel ve hücre tipi spesifik ekspresyon .
- İnsan D-amino asit oksidazın karakterizasyonu .
- D-amino-asit oksidaz, sıçan beynindeki alt beyin sapı ve beyincik ile sınırlıdır: astrositlerin bölgesel farklılaşması .
- Sıçan beyindeki D-amino asit oksidazın immünositokimyasal lokalizasyonu .
- Memelilerde D-amino asitlerin hassas belirlenmesi ve D-amino-asit oksidaz aktivitesinin miktarları üzerindeki etkisi .
- Tedaviye dirençli şizofreni tedavisinde risperidon ve olanzapine ek farmakoterapi olarak D-serin etkinliği .
- Şizofreninin tedavisi için olanzapine ve risperidona yüksek doz glisin eklenmiştir .
- Şizofreni için sarkosin (N-metilglisin) ve D-serin ilave tedavisinin randomize, çift kör, plasebo kontrollü bir karşılaştırma çalışması .
- Şizofreninin akut alevlenmesi için Sarcosine veya D-serin ek tedavisi: randomize, çift kör, plasebo kontrollü bir çalışma .
- Şizofreni tedavisinde yüksek doz D-serin .
- D-serin adjuvan tedavi, Parkinson hastalığında davranışsal ve motor semptomları hafifletir .
- Travma sonrası stres bozukluğunun tedavisi için D-serin pilot kontrollü çalışma .
- Normal ve Alzheimer insan beyninde serbest D-serin konsantrasyonu .
- İnsan temporal korteksinde N-metil-D-aspartatla ilişkili glisin reseptörü agonisti olan D-serin’in varlığı: normal, Parkinson ve Alzheimer dokularının karşılaştırılması .
- Nöropsikiyatrik hastalıklar olan ve olmayan bireylerin post-mortem beyin ve omuriliklerinde serbest D-serin .
- Serin rasemaz, bir alfa, beta eliminasyon aktivitesi aracılığıyla hücre içi D-serin seviyelerini modüle eder .
- Kronik D-Yüksekliğinin Yükselmesinin Depresyon ve Anksiyeteye Bağlı Davranışın Hayvan Modelleri Üzerine Etkileri .
- HPLC kullanımı ile serebrospinal sıvıda D ve L-serinin eşzamanlı analizi .
- İlaç saf şizofreni hastalarının beyin omurilik sıvısında toplam D-serin oranı azaltıldı .
- Astrositler, glutamatın düzenlenmiş ekzositozu için yetkin bir vesiküler bölme içerir .
- Glutamat reseptörü aktivasyonu, gliotransmitter D-serinin bir kalsiyum bağımlı ve SNARE proteinine bağımlı salımını tetikler .
- Bir nöromodülatör olarak D-serin: sıçan beyin glia bölgesel ve gelişimsel lokalizasyonlar NMDA reseptörleri benzer .
- Bir gliotransmitter olarak D-serin ve beyin gelişimi ve hastalığında rolleri .
- Astrositler, gliseransmitter vesikülleri d-serin ile doldurmak için yeni bir taşıyıcı kullanır: veziküler sinerji için kanıt .
- Erişkin hipokampal astrositlerde küçük sinaptik benzeri mikroveziklerde L-glutamat ve D-serin’in immünogold tespiti .
- D-Serinliğinin Astrositik Sinaptik Benzeri Olan Vesiküllere Depolanması ve Alınması Gliotransmission’ı Belirler .
- D-serin’in nöronal salımı: hücre dışı D-serin konsantrasyonunu kontrol eden fizyolojik bir yol .
- Asc-1 taşıyıcı yoluyla nöronal D-serin ve glisin salınması, NMDA reseptörüne bağlı sinaptik aktiviteyi düzenler .
- Astrositler D-serine geniş bir kesecikle salınır .
- TRPA1 Kanalları, Kurucu D-Serin Yayılımı ile Astrosit Bazal Kalsiyum Seviyelerinin Düzenleyicileri ve Uzun Dönemli Potansiyeldir .
- Uzun süreli potansiyelizasyon D-serin’in astrositlerden salınmasına bağlıdır .
- İnsan glioblastoma hücrelerinde serin rasemaz aktivitesinin D-serin ve nitrik oksit ile düzenlenmesi .
- İnsan glioblastoma hücrelerinde serin ve nitrik oksit metabolizması arasındaki karşılıklı düzenleme .
- NMDA’nın NOS aktivasyonunda voltaj bağımlı kalsiyum kanalı tutulumu .
- Düşük doz D-serin’in farelerde tanıma ve çalışma belleği üzerindeki etkileri .
- Glisin tranporter-1 blokajı, in vitro ve in vivo sıçan prefrontal kortikal nöronlarındaki NMDA aracılı yanıtları güçlendirir .
- Glisin transporter-1’in (GLYT-1) bloke edilmesi, hipoglosal motornöronlarda NMDA reseptör aracılı sinaptik iletimi güçlendirir .
- Sıçan beyindeki serbest D-serinin varlığı .
- Sıçan Beyninde Endojen D-Serin: N-Metil-d-Aspartat Reseptör-İlişkili Dağılım ve Yaşlanma .
- Glycine kültürlü fare beyin nöronlarında NMDA yanıtını güçlendirir .
- Aktivasyon kinetikleri, N-metil-D-aspartat reseptörü üzerindeki glutamat ve glisin bağlama bölgelerinin sayısını ortaya koymaktadır .
- Klinik nörolojide NMDA reseptörleri: ileriye dönük ek süre .
- D-serin, N-metil-D-aspartat reseptörünün glisin bölgesi için endojen bir liganddır .
- Xenopus oositlerinde birlikte eksprese edilen bir glisin taşıyıcısı ile NMDA reseptör aktivasyonunun kontrolü .
- Hipokampal nöronlarda sinaptik NMDA reseptörlerinin Glisin regülasyonu .
- Potansiyel yeni tip bir antipsikotik olan glisin taşıyıcı-1 SSR504734’ün seçici inhibitörünün nörokimyasal, elektrofizyolojik ve farmakolojik profilleri .
- D-Serine, sıçan CA1 hipokampal piramidal hücrelerinde ve interneronlarda NMDA reseptör fonksiyonunu modüle eder .
- Glisin neokortikal dilimlerdeki NMDA reseptör aracılı sinaptik potansiyelleri artırır .
- D-serin ve serin rasemaz omurgalı retinada bulunur ve NMDA reseptörlerinin fizyolojik aktivasyonuna katkıda bulunur .
- D-Serine sıçan hipokampal nöronlarında AMPA reseptör aracılı akımı inhibe eder .
- Glisinin fare kortikal kültürlerinde NMDA ile indüklenen nörotoksisite üzerindeki ikili etkisi .
- Glisinerjik inhibitör sinaps .
- Glisin taşıyıcıları: Sinaptik iletimin temel düzenleyicileri .
- Glycine taşıyıcıları: gen silme ile ortaya çıkan farmakolojik ilginin önemli rolleri .
- C6 glioma hücrelerinde D- ve L-serinin alımı .
- Nöromodülatör D-serin’in glial taşınması .
- Oksidatif stres, glutamat ve nörodejeneratif bozukluklar .
- Steroidal olmayan antienflamatuvar ilaçların D-serin kaynaklı oksidatif stres üzerine in vitro etkileri .
- D-serin tedavisi sıçan beyninde oksidatif strese neden olur .
- d-Serin uygulama lipid oksidasyonunu tetikler ve sıçan striatumundaki antioksidan savunmayı azaltır .
- Sıçanlarda geçici ve kalıcı orta serebral arter tıkanıklığından sonra siklooksijenaz-2 haberci RNA’nın indüksiyonu: in situ hibridizasyon kullanılarak c-fos messenger RNA ile karşılaştırma .
- Fokal serebral iskemide siklo-oksijenaz-2 haberci RNA indüksiyonu .
- Deneysel travmatik beyin hasarı sonrası bölgesel ekspresyon ve siklooksijenaz-2’nin rolü
- Alzheimer hastalığında siklooksijenaz ve enflamasyon: deneysel yaklaşımlar ve klinik müdahaleler .
- Siklooksijenaz-2, birincil kortikal hücre kültüründe N-metil-D-aspartat aracılı nöronal hücre ölümüne katkıda bulunur .
- Bellekte sinaptik plastisitenin rolünün moleküler ve hücresel bilişsel çalışmaları .
- Moleküler ve hücresel bilişe genetik yaklaşımlar: LTP’ye odaklanma, öğrenme ve hafıza .
- Farelerde öğrenme ve hafıza genetik artırılması .
- Siklin bağımlı kinaz 5, NMDAR bozunmasının kontrolü yoluyla öğrenme ve sinaptik plastisiteyi yönetir .
- Glia’dan elde edilen D-serin, NMDA reseptör aktivitesini ve sinaptik hafızayı kontrol eder .
- Uzun süreli depresyon: öğrenme için hücresel bir temel .
- D-serin, NMDA-NR2B reseptör bağımlı hipokampal uzun süreli depresyon ve mekansal geri dönüşüm öğrenme artırır .
- Hipokampal uzun süreli depresyon ve mekansal hafıza geri kazanımı üzerinde çan şeklinde D-serin etkileri .
- Genç ve yaşlı sıçanların hipokampal dilimlerindeki yüksek Mg2 + -to-Ca2 + oranlarının frekans potansiyeline etkileri .
- Yaşlı, bellek yetersizliği olan sıçanlardan in vitro hipokampal dilimlerdeki bozulmuş monosinaptik potansiasyon .
- Kalsiyum homeostazisi ve yaşlı beyinde sinaptik plastisite modülasyonu .
- Beyindeki yaşlanma ve Alzheimer hastalığının kalsiyum hipotezinin genişlemesi: Mağazayı önemsemek .